
【题目】霞石是一种硅酸盐,其组成可表示为K2O·3Na2O·4Al2O3·8SiO2,某小组同学设计以霞石为原料制备Al2O3的方案如下:

请回答下列问题:
(1)沉淀1的化学式为______________________________________________。
(2)滤液1与过量NaOH溶液反应的所有的离子方程式为____________。
(3)写出由溶液2生成Al(OH)3的离子方程式:_______________________。
(4)通入过量的CO2,过滤后的滤液中含有的阴离子主要是________。
(5)由Al(OH)3→Al2O3的反应条件为_________________________________。
【答案】SiO2H++OH-===H2O、Al3++4OH-===AlO2-+2H2OAlO2-+CO2+2H2O===Al(OH)3↓+HCO3-Cl-、HCO3-高温
【解析】
由霞石为原料制备Al2O3的方案可知,霞石中加盐酸,只有二氧化硅不反应,则沉淀I为SiO2,滤液I中含氯化钾、氯化钠、氯化铝、HCl,再加过量的NaOH,发生酸碱中和、氯化铝与NaOH反应生成偏铝酸钠,再通入二氧化碳,偏铝酸钠与二氧化碳反应生成氢氧化铝沉淀,过滤后加热氢氧化铝可制备氧化铝,据此解答。
(1)由上述分析可知,沉淀I为SiO2;
(2)向滤液1中含氯化钾、氯化钠、氯化铝、HCl,因此加入过量NaOH溶液的有关反应离子方程式为H++OH-=H2O、Al3++4OH-=AlO2-+2H2O;
(3)由溶液2中含有偏铝酸钠,通入过量二氧化碳生成Al(OH)3的离子方程式为AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-;
(4)滤液里主要的阴离子为滤液1中本身含有的氯离子以及通入过量CO2后生成的HCO3-;
(5)Al(OH)3受热易分解,选择高温加热可使Al(OH)3分解生成Al2O3。


 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源: 题型:
【题目】醋酸溶液中存在电离平衡:CH3COOH![]() H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
A. 醋酸溶液中离子浓度的关系满足:c(H+)= c(CH3COO-)+c(OH-)
B. 物质的量浓度相等CH3COOH和CH3COONa混合溶液:c(CH3COO-)-c(CH3COOH)=2c(H+)-2c(OH-)
C. CH3COOH溶液加水稀释 不变
不变
D. CH.COOH溶液加水稀释,溶液中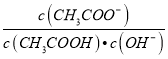 不变
不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把一块镁铝合金投入到过量的1 mol·L-1盐酸中,待合金完全溶解后,再往溶液里加入1 mol·L-1NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图所示,下列说法中错误的是( )
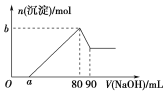
A. 盐酸的体积为90 mL
B. a的取值范围为0<a<50
C. n(Mg2+)<0.025 mol
D. 当a值为30时,b值为0.02
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度和有催化剂条件下,恒容密闭容器中发生反应N2+3H2 2NH3,下列说法正确的是( )
t/min | 0 | 5 | 10 | 15 | 20 |
c(NH3)/(mol·L-1) | 0 | 1.00 | 1.60 | 1.80 | 1.80 |
A. 0~10min内,v(NH3)=0.16mol·L-1·min-1 B. 0~10min内,v(N2)=0.18mol·L-1·min-1
C. 0~10min内,v(N2)=0.16mol·L-1·min-1 D. 15~20min内,反应v(N2)正= v(N2)逆=0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家利用太阳能分解水生成的氢气在催化剂作用下与二氧化碳反应生成甲醇,并开发出直接以甲醇为燃料的燃料电池。已知H2(g)、CO(g)和CH3OH(l)的燃烧热△H分别为—285.8kJ·mol-1、—283.0kJ·mol-1和—726.5kJ·mol-1。请回答下列问题:
(1)用太阳能分解10mol水消耗的能量是_____________;
(2)甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为_______________________________________________________;
(3)在容积为2L的密闭容器中,由CO2和H2合成甲醇,在其他条件不变的情况下,考查温度对反应的影响,实验结果如下图所示(注:T1、T2均大于300℃);
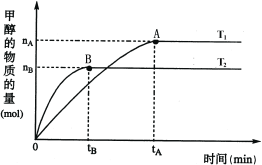
下列说法正确的是________(填序号)
a.温度为T1时,从反应开始到平衡,生成甲醇的平均速率为:v(CH3OH)=![]() mol·L-1·min-1
mol·L-1·min-1
b.T1> T2
c.该反应为放热反应
d.处于A点的反应体系从T1变到T2,达到平衡时![]() 增大
增大
(4)在T1温度时,将1molCO2和3molH2充入一密闭恒容器中,充分反应达到平衡后,若CO2转化率为α, 则容器内的压强与起始压强之比为_______________________;
(5)在直接以甲醇为燃料的电池中,电解质溶液为碱性,负极的反应式为________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组反应中,属于可逆反应的一组是( )
A. 2H2O![]() 2H2↑+O2↑,2H2+O2
2H2↑+O2↑,2H2+O2![]() 2H2O
2H2O
B. NH3+CO2+H2O=NH4HCO3,NH4HCO3![]() NH3↑+H2O↑+CO2↑
NH3↑+H2O↑+CO2↑
C. H2+I2![]() 2HI,2HI
2HI,2HI![]() H2↑+I2↑
H2↑+I2↑
D. 2Ag+Br2![]() 2AgBr,2AgBr
2AgBr,2AgBr![]() 2Ag+Br2
2Ag+Br2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com