
 ʵ�����Ʊ�����ͪ�Ļ�ѧ����ʽΪ��
ʵ�����Ʊ�����ͪ�Ļ�ѧ����ʽΪ��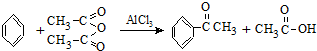
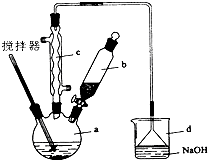
���� ����������Ӧԭ���Ʊ�����ͪ����Ӧ������Ҫ���Ʒ�Ӧ�¶Ȳ�������Ӧ�����������߷�Ӧ��������ʣ��ռ�������Ҫ��ȫ��ʩ���ռ�������������з����ᴿ���漰��Һ������Ҫ�㣻
��1����Ӧ��ϼ���ʱ���ӷ������û��cװ�û�������������һ�𣬼����˷����ᴿ�Ѷȣ��ҷ�Ӧ��������ʵͣ�������cװ��ͨ�������������»ص���Ӧ�����У�װ��d���ռ�����ͪ���õ��õ�����©���ﵽ��������Ŀ�ģ�
��2������ͪҲ������ˮ�����ñ���ȡ�ɼ��ٲ������ʧ��������ȡԭ�������������ڻ������ܵ��ܼ��е��ܽ�Ȳ�ͬ���Ի����Һ���з��룻
��3����Һ©��������ǻ������ܵ�Һ������ɽ�ϲ����ı��ʺ�ע�������жϣ�
��� �⣺��1��װ��c�������ܣ��ɽ����Ȼӷ����ı������������»�������Ӧ�����У������ԭ�ϵ������ʣ�Ҳ����������ķ����ᴿ�Ѷȣ�dװ�������õ��õ�����©���ռ�����ͪ���������˽��������Ҳ�ﵽ��������Ŀ�ģ��ʴ�Ϊ����������ԭ�ϣ���ֹ������
��2��ˮ���ñ���ȡ����Һ��Ŀ���ǰ��ܽ���ˮ�еı���ͪ��ȡ�����Լ�����ʧ�������Ҵ�����ˮ���ܲ��ֲ㣬���Բ����þƾ����汽������ȡ�������ʴ�Ϊ�����ܽ���ˮ�еı���ͪ��ȡ�����Լ�����ʧ���Ҵ���ˮ���ܣ�
��3���ñ���ȡʱ���ܶ�С�����÷ֲ�������ϲ㣬��Һ©������Ļ�����ֻ�����²�Һ���������ϲ㱽��Ӵӷ�Һ©���Ͽڵ������ʴ�Ϊ���ϣ��ӷ�Һ©���Ͽڵ�����
�ʴ�Ϊ����©�����������Ͽڲ�������
���� ���⿼���������Ʊ������롢�ᴿ����ȡ��ѡ������ʹ�õ��������֪ʶ��Ӧ�ã���ѧʵ�����֪ʶ�ͻ������ܵ������ǽ���ؼ�����Ŀ�Ѷ��еȣ�


 ������ĩ��ϰ��ѵ��ϵ�д�
������ĩ��ϰ��ѵ��ϵ�д� С��ʿ��ĩ����100��ϵ�д�
С��ʿ��ĩ����100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ʢ��10mLˮ����Ͳ�е���Ũ���ἴ��ϡ���� | |
| B�� | ���Թ��еμ��Լ�ʱ�����ι��¶˽����Թ��ڱ� | |
| C�� | ʹ����ֽ������Һ������ʱ������ֽ������Һ�� | |
| D�� | ��������ƽ����ҩƷʱ�����̷�ҩƷ�����̷����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | M��A����ʹ���Ը��������Һ����ˮ��ɫ | |
| B�� | B�ܷ�����ȥ��������ȡ�������۵ȷ�Ӧ | |
| C�� | 1molM�������ռ���Һ��Ӧ��������2nmolNaOH | |
| D�� | A��B��C��1mol�ֱ�������Ʒ�Ӧ���ų���������ʵ���֮��Ϊ1��2��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1L1mol•L-1��Na2CO3��Һ�к���CO32-����ĿΪNA | |
| B�� | 28g����ϩ�ͱ�ϩ�к�̼ԭ����ĿΪNA | |
| C�� | ��״���£�6.72LNO2��ˮ��ַ�Ӧת�Ƶĵ�����ĿΪ0.1NA | |
| D�� | ���³�ѹ�£�14g��N2��CO��ɻ�����庬�е�ԭ����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ʵ������ijʵ��С��ͬѧ��������ͭ����ȡ��Ӧ�ã����������ʵ�飺
��ʵ������ijʵ��С��ͬѧ��������ͭ����ȡ��Ӧ�ã����������ʵ�飺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
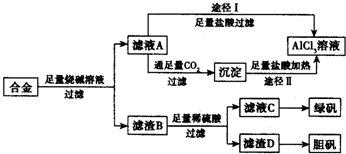 ��ҵ���ú�����������ͭ�ĺϽ�ҵ������ȡ�������Ȼ�����Һ���̷����壨FeSO4•7H2O�� �͵������壨CuSO4•5H2O����������·�����ͼ��ʾ����ش�������⣺
��ҵ���ú�����������ͭ�ĺϽ�ҵ������ȡ�������Ȼ�����Һ���̷����壨FeSO4•7H2O�� �͵������壨CuSO4•5H2O����������·�����ͼ��ʾ����ش�������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������̼���������ЧӦ����Ҫ���壬������̼�Ļ����������Ǽ�������ЧӦ����Ч;��֮һ��
������̼���������ЧӦ����Ҫ���壬������̼�Ļ����������Ǽ�������ЧӦ����Ч;��֮һ��| �¶�/K CO2ת����/% a/mol | 500 | 600 | 700 | 800 |
| 1.67 | x | 33 | ||
| 1.25 | 60 | 43 | y | |
| 0.83 | z | 32 | w |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
 �¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������
�¶�ΪTʱ����2.0L�����ܱ������г���1.0mol PCl5����ӦPCl5��g��?PCl3��g��+Cl2��g������һ��ʱ���ﵽƽ�⣮��Ӧ�����вⶨ��n��PCl3����ʱ��ı仯��ͼ������˵����ȷ���ǣ�������| A�� | ��Ӧ��ǰ50s��ƽ������v��PCl5��=0.0032 mol•L-1•s-1 | |
| B�� | �÷�Ӧ��ƽ�ⳣ��K=0.025 | |
| C�� | ��ͬ�¶��£���ʼʱ�������г���1.0molPCl5��0.20molPCl3 ��0.20mol Cl2����Ӧ�ﵽƽ��ǰv��������v���棩 | |
| D�� | ���������������䣬�����¶ȣ�ƽ��ʱ��c��PCl3��=0.11mol•L-1����Ӧ�ġ�H��0 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com