
 CH3OH + H2O)
CH3OH + H2O)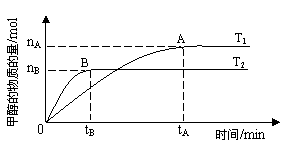
 ��
��


| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Cd(OH)2 + 2Ni(OH)2����֪Ni(OH)2��Cd(OH)2��
Cd(OH)2 + 2Ni(OH)2����֪Ni(OH)2��Cd(OH)2��| A���ŵ�ʱ������Cd��2e����Cd2+ |
| B���ŵ�ʱ������2NiOOH + 2e�� + 2H2O��2Ni(OH)2 + 2OH�� |
| C�����ʱ������2Ni(OH)2��2e��+ 4H+��2Ni3+ + 4H2O |
| D�����ʱ������Cd(OH)2 + 2e����Cd + 2OH�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
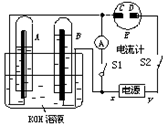
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2PbSO4��2H2O��������������ȷ����(����)
2PbSO4��2H2O��������������ȷ����(����)| A��Pb������ | B��PbO2�õ��ӣ������� |
| C��PbO2�õ��ӣ�����ԭ | D����طŵ�ʱ����Һ������ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2Na+xS������˵����ȷ����
2Na+xS������˵����ȷ����| A���ŵ�ʱ��Na ��������S��������ԭ��Ӧ |
| B�����ʱ�Ƽ������Դ���������� |
| C�����øõ�ص��AgNO3��Һʱ�������ϲ�����״��������11.2Lʱ�����Ľ�����2.3g |
| D�����ʱ�����������ķ�ӦΪ��Sx2--2e�� = xS |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������������mg����ʱ����������ͬʱ��mg�������� |
| B����ص�������ӦʽΪ��O2 + 2H2O + 4e���� 4OH�� |
| C������c(Na+)/c(CO32-) ��ֵ���䣬����ҺpH���ֲ��� |
| D�����һ��ʱ�䣬����ָ�Na2CO3ԭŨ�ȣ�ֻ��Ҫ����ˮ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Li2S2O4�������йظõ�ص�˵����ȷ���ǣ� ��
Li2S2O4�������йظõ�ص�˵����ȷ���ǣ� ��| A���ŵ�Li+�������ƶ� |
| B���õ���ܼ�����ˮ��� |
| C���õ�طŵ�ʱ��1mol SO2���뷴Ӧ��ת��2mol e- |
| D�����������ӦʽΪ2Li++2SO2+2e-=Li2S2O4 |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com