
右图是某老师设计的一个微型实验装置图,请你说出实验过程中可能出现的现象,试写出有关化学方程式。
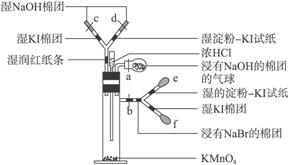
图中a、b、c、d均为止水夹,e、f为红皮头
①出现黄绿色气体:2KMnO4+16HCl====2KCl+ 2MnCl2+5Cl2↑+8H2O;
②湿润的红纸条褪色:Cl2+H2O![]() HCl+ HClO;
HCl+ HClO;
③c处湿碘化钾棉团变为棕褐色:Cl2+2KI====2KCl+ I2;
④b附近浸有湿溴化钠的棉团变黄色:Cl2+2NaBr====2NaCl+Br2;
e、f处的现象分别为变蓝色(因含有淀粉)和棕褐色:Br2+ 2KI====2KBr+I2;
⑤d处的现象、原因均同e处:Cl2+2KI====2KCl+I2;
⑥湿的氢氧化钠棉花团均先变淡黄绿色后又褪色:Cl2+2NaOH====NaCl+NaClO+H2O
本装置将氯气的制取与卤素间的置换反应有机地结合起来,把氯气、溴蒸气及单质碘之间的相互关系充分地体现了出来,整套装置浑然一体,实验现象明显直观,各种性质由于颜色的明显变化而一目了然,实验药品用量较少,实验过程气体不外漏,不仅可节约药品,而且绿色环保。有利于培养学生的创造性思维和综合运用知识的能力。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
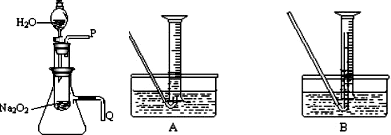 (2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.
(2008?枣庄一模)化学课上老师做了一个演示实验:用脱脂棉包住约0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴水,观察到脱脂棉剧烈燃烧起来.查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
 (2012?宜春模拟)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如图所示:
(2012?宜春模拟)硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如图所示:| 实验 小组 |
称取CuSO4 的质量/g |
仪器C增 加的质量/g |
量筒中水的体积折算标 准状况下气体的体积/mL |
| ① | 6.4 | 2.56 | 224 |
| ② | 6.4 | 2.56 | 448 |
| ||
| ||
| 10 |
| 9 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
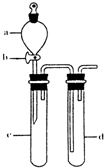 SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.
SO2是一种重要的化工原料,也是引起酸雨污染的重要来源.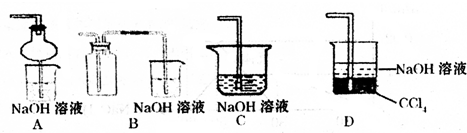
查看答案和解析>>
科目:高中化学 来源: 题型:
某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用右图装置,对获得的铜粉(含炭)样品进行实验。图中铁架台等装置已略去。请你帮助他们完成下列实验报告。
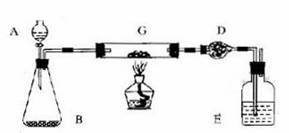
(一)实验目的:__________________________________。
(二)实验用品:仪器:天平、分液漏斗、锥形瓶、硬玻璃管、干燥管、酒精灯、洗气瓶等
药品:红褐色铜粉(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰。浓硫酸等
(三)实验内容:
| 实验过程 | 实验现象 | 有关化学方程式 |
| 在C中加入样品标本W克,D中装入精品后并称量为m克。连接好仪器后,检查气密性 | --------------------------------- | ---------------------------- |
| 打开A的活塞,慢慢洋加溶液。 | ||
| 对G进行加热。当G中药品充分反应后。关闭A的活塞。停止加热: | ||
| 冷却后,称量D的质量为m2克。 | --------------------- | ------------------ |
(四)计算:样品中铜的质量分数=________________(用含W、m1、m2的代数式表示)
(五)问题和讨论:
实验完成后,老师评议说:按上述实验设计,即使G中反应完全、D中吸收完全,也不会得出正确的结果。经讨论,有同学提出在B与G之间加入一个装置。再次实验后,得到了较正确的结果。那么,原来实验所测得的钢的质量分数偏小的原因可能是_______________-,在B与G之间加入的装置可以是________________,其中盛放的药品是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com