
【题目】下列说法正确的是( )
A. 反应物分子的每次碰撞都能发生化学反应
B. 活化分子之间的碰撞一定是有效碰撞
C. 能够发生化学反应的碰撞是有效碰撞
D. 增大反应物浓度时,活化分子百分数增大
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】组成小麦的主要元素是( )
A. C、H、Ca、K、Mg、B
B. N、P、S、Zn、Cu、Mn
C. C、H、O、P、S、N
D. H、O、Fe、B、Zn、Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】猫头鹰体内有A种蛋白质,20种氨基酸;田鼠体内有B种蛋白质,20种氨基酸。猫头鹰捕食田鼠一小时后其消化道中的小肠上皮细胞中含有蛋白质种类和氨基酸种类最可能是( )
A. A+B,40 B. A,20 C. >A,20 D. <A,20
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行如下反应:2X(g) + Y(g) ![]() Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是( )
A.达到平衡时X浓度为0.04 mol/L
B.将容器体积变为20 L,Z的平衡浓度变为0.015mol/L
C.若增大压强,平衡向正方向移动,平衡常数变大
D.若升高温度,X的体积分数增大,则该反应的H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用离子方程式解释以下指定反应,书写正确的是( )
A. 亚硫酸钠溶液显碱性:SO32-+2H2O=H2SO3+2OH-
B. (NH4)2FeSO4溶液与过量NaOH溶液混合制取氢氧化亚铁:Fe2++2OH-=Fe(OH)2
C. NaAlO2溶液中通入过量CO2制取氢氧化铝:2AlO2-+CO2+3H2O=2Al(OH)3+CO32-
D. 铁红溶于HI酸溶液:Fe2O3+6H++2I-=2Fe2++I2+3H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法不正确的是( )
A.4.6g金属钠与足量O2充分反应后,所得固体中阴、阳离子的总数为0.3NA
B.1L 0.5 mol/L的FeCl3溶液充分水解后,所得Fe(OH)3胶粒的数目为0.5NA
C.2.0g H218O与D2O的混合物中所含中子数为NA
D.1L含NA个Al3+的Al(NO3)3液中,NO3﹣物质的量浓度大于3 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应3Fe(s)+4H2O(g) ![]() Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
Fe3O4(s)+4H2(g)的平衡常数,下列说法正确的是( )
A.K=![]()
B.K=![]()
C.增大c(H2O)或减小c(H2),会使该反应平衡常数减小
D.改变反应的温度,平衡常数不一定变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(原创)下列事实能用勒夏特列原理解释的是
A.使用催化剂,在单位时间内提高合成氨产率
B.对于2HI(g) ![]() H2(g)+2CO(g),达平衡后.缩小容器体积可使体系颜色变深
H2(g)+2CO(g),达平衡后.缩小容器体积可使体系颜色变深
C.对于2CaO2(s) ![]() 2CaO(s)+O2(g),达平衡后增大压强,再次平衡后O2的浓度保持不变
2CaO(s)+O2(g),达平衡后增大压强,再次平衡后O2的浓度保持不变
D.溴水中有下列平衡:Br(aq)+ H2O(l) ![]() HBr(aq)+HBrO(aq)当加入硝酸银溶液后,溶液颜色变浅
HBr(aq)+HBrO(aq)当加入硝酸银溶液后,溶液颜色变浅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温下,Al(OH)3的Ksp或溶解度远大于Fe(OH)3。向浓度均为0.1 mol·L-1的Fe(NO3)3和Al(NO3)3混合溶液中,逐滴加入NaOH溶液。下列示意图表示生成Al(OH)3的物质的量与加入NaOH溶液的体积的关系,合理的是( )
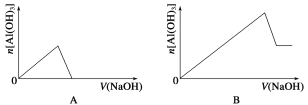
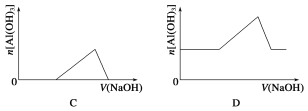
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com