
| A、Z元素在反应①中被氧化,在③中被还原 |
| B、还原性强弱顺序为:X2+<Z-<R-<M2+ |
| C、氧化性强弱顺序为:XO4-<Z2<R2<M |
| D、常温下不可发生反应2M2++Z2=2M3++2Z- |


科目:高中化学 来源: 题型:

| A、图1说明烯烃与H2的加成反应是放热反应,虚线表示在有催化剂的条件下进行 |
| B、向盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液,产生的沉淀质量m与加入的体积V之间的关系有可能是图2 |
| C、图3表示KNO3的溶解度曲线,图中a点所示的溶液在80℃时不可能存在 |
| D、在体积相同的两个密闭容器中,分别充入等质量的O2和X气体,由图4可确定X可能是CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将Cl2通入品红溶液 | 溶液红色褪去 | Cl2具有较强还原性 |
| B | 常温下将Fe片放入稀硝酸中 | 产生无色可燃气体 | Fe与稀硝酸反应放出H2 |
| C | 往Na2CO3溶液中滴加稀盐酸,边滴边振荡 | 溶液开始无气泡产生, 需滴加一定量盐酸才能产生气泡 | CO32-+H+=HCO3- HCO3-+H+=H2O+CO2↑ |
| D | 往硫酸铝溶液通入过量氨气 | 产生白色沉淀 | Al(OH)3不溶于氨水 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、气态氢化物的稳定性:X<Z<W |
| B、Y的阳离子半径比W的阴离子半径小 |
| C、X、Z、W氧化物对应水化物酸性的强弱顺序为Z<X<W |
| D、室温下,含Y元素的盐形成的水溶液其pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素代号 | X | Y | Z | M | N | R | Q | |
| 原子半径(×10-10m) | 1.86 | 0.99 | 1.43 | 1.60 | 1.02 | 0.75 | 0.74 | |
| 主要化合价 | 最高正价 | +1 | +7 | +3 | +2 | +6 | +5 | -- |
| 最低负价 | -- | -1 | -- | -- | -2 | -3 | -2 | |
| A、气态氢化物的稳定性:N>Y |
| B、元素X和Q形成的化合物中不可能含有共价键 |
| C、M(OH)2的碱性比XOH的碱性强 |
| D、X、Z、R的最高价氧化物对应的水化物之间可两两相互反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、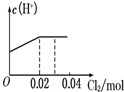 |
B、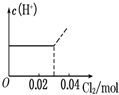 |
C、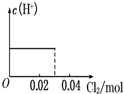 |
D、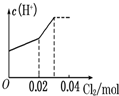 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡常数K的大小能说明反应的限度,因此当平衡右移时,K值必定增大 |
| B、可逆反应达到平衡状态后,改变外界条件后,若反应速率发生变化,则平衡一定发生移动 |
| C、若反应2A(g)+B(g)?2C(g)是自发反应,则该反应的△H<0 |
| D、使用催化剂可降低反应活化能,加快反应速率,改变反应限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com