
【题目】某有机物在氧气中充分燃烧,生成水蒸气和CO2的物质的量之比为1∶1,由此可以得出的结论是( )
A.该有机物分子中C、H、O原子个数比为1∶2∶3B.分子中C、H原子个数比为1∶2
C.有机物中必定含有氧D.有机物中必定不含有氧
科目:高中化学 来源: 题型:
【题目】纳米TiO2在涂料、光催化、化妆品等领域有着极其广泛的应用。制备纳米TiO2的方法之一是TiCl4水解生成TiO2·xH2O,经过滤、水洗除去其中的Cl-,再烘干、焙烧除去水分得到固体TiO2。实验室用氧化还原滴定法测定TiO2的质量分数:一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。请回答下列问题:
(1)TiCl4水解生成TiO2·xH2O的化学方程式为_________________________________。
(2)配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4的原因是_________________________。
(3)NH4Fe(SO4)2标准溶液盛装在___________(填“酸式”或“碱式”)滴定管中,滴定终点的现象是________________________。若在滴定终点读取滴定管刻度时,仰视标准液液面使测定结果________(填“偏高”“偏低”或“无影响”)。
(4)滴定分析时,称取TiO2(摩尔质量为Mg·mol-1)试样w g,消耗c mol·L-1 NH4Fe(SO4)2标准溶液VmL,则TiO2质量分数表达式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(题文)某有机物(含C、H、O三种元素)分子球棍模型如图所示,下列有关叙述正确的是

A. 分子式为C9H6O3
B. 不能使酸性KMnO4溶液褪色
C. 最多能与含1molNaOH的溶液反应
D. 能与碳酸氢钠溶液反应放出CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z三种物质存在如图所示的转化关系(图中“→”表示一步转化)。下列各组物质中,不能满足此转化关系的是( )
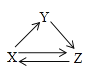
物质 选项 | X | Y | Z |
A | Al | Al2O3 | NaAlO2 |
B | Fe | FeCl3 | FeCl2 |
C | C | CO | CO2 |
D | Cl2 | HCl | NaCl |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物有如下转化关系:

(1)写出反应A→B的反应条件是____________,C中官能团的结构简式是______________。
(2)写出反应B→C的化学方程式和反应类型:_______________,反应类型为____________。
(3) 在浓硫酸加热条件可以生成含有三个六元环结构的有机物,该有机物结构简式为:____________。
在浓硫酸加热条件可以生成含有三个六元环结构的有机物,该有机物结构简式为:____________。
(4)写出符合下列条件的C的同分异构体的结构简式______________、_____________。
①属于芳香族化合物,苯环上有两个取代基
②与碳酸氢钠溶液反应放出二氧化碳气体
③苯环上的一氯代物有两种
(5)写出以 和CH3CH2Cl,为原料合成重要的化工产品
和CH3CH2Cl,为原料合成重要的化工产品![]() 的路线流程图(无机试剂任选)______。
的路线流程图(无机试剂任选)______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴乙烷是有机合成中的重要原料。实验室制备溴乙烷(C2H5Br,沸点38.4℃)的装置如图所示,其实验步骤为:①检查装置的气密性,向装置图所示的U形管和大烧杯中加入冰水;②向仪器a中加入10mL 95%乙醇、28mL 92%浓硫酸,然后加入适量溴化钠和几粒碎瓷片;③在45~50℃加热2h,使其充分反应。回答下列问题:
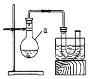
(1)仪器a的名称是________。
(2)在大烧杯中加入冰水的目的是________。
(3)加入碎瓷片的作用是________。
(4)为了更好的控制温度,选择常用的加热方式为________。
(5)反应时若温度过高,可看到有红棕色气体产生,该气体分子式为________,生成的无色刺激性气味气体的分子式为________。
(6)U形管内可观察到的现象是_____________。
(7)反应结束后,U形管内粗制的C2H5Br呈棕黄色。为了除去粗产品中的杂质,可以选择下列试剂中的________(填序号)。
A.Na2SO3溶液 B.H2O C.NaOH溶液 D.苯
(8)检验溴乙烷中溴元素的实验步骤是:取少量溴乙烷于试管中,加入NaOH溶液,加热煮沸一段时间,冷却,________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知拆开1molHH键、1mol II键、1molHI键分别需要吸收的能量为436kJ、151kJ、299k J.则由氢气和碘反应生成1mol HI需要______(填“放出”或“吸收”)______kJ的热量.氢气、碘和碘化氢三种分子最稳定的是______(填化学式)
(2)C、![]() 是常用的燃料,它们每1mol分别完全燃烧生成
是常用的燃料,它们每1mol分别完全燃烧生成![]() 及
及![]() 时,放出的热量分别为
时,放出的热量分别为![]() 、
、![]() 。计算说明:
。计算说明:![]() 有数值计算的题,数值结果保留到小数点后1位。
有数值计算的题,数值结果保留到小数点后1位。![]()
![]() 完全燃烧时放出的热量?_________
完全燃烧时放出的热量?_________
![]() 完全燃烧相同质量的C和
完全燃烧相同质量的C和![]() ,哪种燃料放出热量较多?_________
,哪种燃料放出热量较多?_________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列指定反应的离子方程式正确的是( )
A. 向NaHCO3溶液中加足量Ba(OH)2溶液:HCO3-+Ba2++OH-=BaCO3↓+H2O
B. Cu溶于稀硝酸:Cu+2H++NO3-=Cu2++NO2↑+H2O
C. 酸性溶液中KIO3与KI反应生成I2:IO3-+I-+6H+=I2+3H2O
D. 氯气溶于水:Cl2+H2O=H++Cl-+HClO
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据要求回答下列问题:
(1).①H、D、T ②H2O、D2O ③石墨、金刚石 ④ 和
和 四组微粒或物质中,互为同位素的是_______;(填序号,下同)互为同分异构体的是_____。
四组微粒或物质中,互为同位素的是_______;(填序号,下同)互为同分异构体的是_____。
(2).甲烷是无色、无味的气体,不溶于水,是天然气、沼气(坑气)的主要成分。甲烷______(填写“能”或“不能”)使酸性高锰酸溶液褪色。在光照条件下,甲烷和氯气能发生反应,此化学反应的类型为_____________ ,请写出甲烷和氯气反应生成一氯甲烷的化学方程式________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com