
| 40g |
| 32g/mol |
| c(NH3)2 |
| c(H2)3.c(N2) |
| 40g |
| 32g/mol |
| 2.25mol |
| 6mol |
| c(NH3)2 |
| c(H2)3.c(N2) |
(
| ||||
|


 提分百分百检测卷系列答案
提分百分百检测卷系列答案科目:高中化学 来源: 题型:

| 元素编号 元素性质 |
① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 |
| 最高增化合价 | +2 | +1 | +5 | +7 | +1 | +5 | |
| 最低化合价 | -2 | -3 | -1 | -3 |
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
(18分)已知镁在空气中燃烧主要生成氧化镁,同时还会与氮气反应生成微量的氮化镁(Mg3N2)在周期表中,镁与锂;铍与铝处于对角线上,处于对角线上的主族元素性质相 似,这称为对角线规则。据此请回答:
(1) 锂在空气中燃烧主要产物的电子式是 _______同时生成微量的_____ _______。(写化学式)
(2)铍的最高价氧化物对应的水化物的化学式是_________________,它属两性化合物,
证明这一结论的有关离子方程式为______________________ _,__________ ______________。
(3)若已知反应Be2C+4H2O===2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式
为________________________________________________。
(4) 用电子式表示BeCl2的形成过程:________________________________________。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年四川省树德协进中学高二上学期期中考试化学试卷 题型:填空题
(18分)已知镁在空气中燃烧主要生成氧化镁,同时还会与氮气反应生成微量的氮化镁(Mg3N2)在周期表中,镁与锂;铍与铝处于对角线上,处于对角线 上的主族元素性质相 似,这称为对角线规则。据此请回答:
上的主族元素性质相 似,这称为对角线规则。据此请回答:
(1) 锂在空气中燃烧主要产物的电子式是 _______同时生成微量的_____ _______。(写化学式)
(2)铍的最高价氧化物对应的水化物的化学式是_________________,它属两性化合物,
证明这一结论的有关离子方程式为______________________ _,__________ ______________。
(3)若已知反应Be2C+4H2O===2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式
为________________________________________________。
(4) 用电子式表示BeCl2的形成过程:________________________________________。
查看答案和解析>>
科目:高中化学 来源:2013届四川省高二上学期期中考试化学试卷 题型:填空题
(18分)已知镁在空气中燃烧主要生成氧化镁,同时还会与氮气反应生成微量的氮化镁(Mg3N2)在周期表中,镁与锂;铍与铝处于对角线上,处于对角线上的主族元素性质相 似,这称为对角线规则。据此请回答:
(1) 锂在空气中燃烧主要产物的电子式是 _______ 同时生成微量的_____ _______。(写化学式)
(2)铍的最高价氧化物对应的水化物的化学式是_________________,它属两性化合物,
证明这一结论的有关离子方程式为______________________ _,__________ ______________。
(3)若已知反应Be2C+4H2O===2Be(OH)2+CH4↑,则Al4C3遇强碱溶液反应的离子方程式
为________________________________________________。
(4) 用电子式表示BeCl2的形成过程:________________________________________。
查看答案和解析>>
科目:高中化学 来源:2014届河北省高一下学期期中考试化学试卷(解析版) 题型:填空题
(16分)A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大。A原子核内无中子;A和E、D和F分别同主族,且B与D 最外层电子数之比为2:3。试回答下列问题:
(1)A元素的名称是 ,E元素在周期表中的位置是 ;
(2)C、D、F的气态氢化物稳定性由强到弱的顺序是 (填化学式);
(3)E单质在足量D单质中燃烧生成的化合物的电子式是 ;
(4)化合物X、Y均由A、D、E、F四种元素组成。
①X、Y均属于 化合物(填“离子”或“共价”);
②X与Y的水溶液相混合发生反应的离子方程式为 ;
(5)化合物E2F的水溶液中滴入双氧水和稀硫酸,加热,有单质生成。其离子反应方程式为: 。
(6)在A2D晶体中,每个分子与相邻的4个分子形成氢键,已知该晶体的升华热(晶体直接变成同温度气体时需要吸收的热量,叫做该晶体的升华热)是51 kJ/mol,除氢键外,分子间还存在范德华力(11 kJ/mol),则该晶体中氢键的“键能”是____kJ/mol;
【解析】原子核内无中子只有H,则A是氢元素。A和E,且E的原子序数大于B、C、D的,所以E只能是Na。B与D 最外层电子数之比为2:3,因为D的原子序数小于Na的所以D位于第二周期。若B与D 最外层电子数就是2和 3,则C就不能存在,所以B与D 最外层电子数就是4和6,即B是C,D是O,则C是N,F是S。
(1)略
(2)非金属性越强,氢化物的稳定性就越强,非金属性是O>N>S。
(3)钠的燃烧产物是过氧化钠,含有离子键和非极性键。
(4)钠是活泼的金属,所以由H、O、Na、S形成的化合物一定是离子化合物,它们分别为NaHSO4和NaHSO3。
(5)Na2S中S的化合价处于最低价态,具有还原性,而双氧水具有氧化性,二者分数氧化还原反应。
(6)每个水分子与相邻的4个分子形成氢键,则平均每个水分子形成的氢键是2个,所以氢键键能是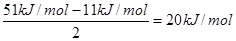 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com