
����Ŀ����֪AΪ������,����Ħ������Ϊ95g��mol-1,DΪ�����,M��һ�ֳ��������壬N��һ�ֳ����������ʡ�����֮���ת����ͼ��ʾ��
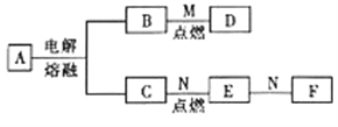
��ش��������⣺
��1��A�Ļ�ѧʽΪ___________��
��2����A����B��C�ķ�Ӧ��,ÿת��1mol����,��������________gB��
��3����֪D�к������ֹ���,��������һ�ֹ��嵥��Ϊ��ɫ,��һ�ֹ���ΪB���������M��Ħ������Ϊ_________g��mol-1��
��4��E��ˮ��Һ��N��Ӧ�����ӷ���ʽΪ___________________________��
���𰸡� MgCl2 12 44 2Fe3++Fe=3Fe2+
�����������������þ�ڶ�����̼������ȼ����������þ��̼������D�к������ֹ���,��������һ�ֹ��嵥��Ϊ��ɫ,��һ�ֹ���ΪB��������������D������þ��̼���ʡ�B��þ���Ȼ�þ��Ħ��������95g��mol-1����������Ȼ�þ����þ������������������ȼ�������Ȼ������Ȼ���������Ӧ�����Ȼ�������
�������������Ϸ�������1��A���Ȼ�þ ����ѧʽΪMgCl2��
��2�����Ȼ�þ�������þ�������ķ�Ӧ����þ��+2�۱�Ϊ0�ۣ�ÿת��1mol��������0.5molþ��������12g��
��3���������Ϸ�����M�Ƕ�����̼��Ħ������Ϊ44g��mol-1��
��4��E���Ȼ������Ȼ�����Һ������Ӧ�����Ȼ����������ӷ���ʽΪ2Fe3++Fe=3Fe2+��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪![]() �DZ�
�DZ�![]() �������ᣬ��ˮ�д�������ƽ�⣺
�������ᣬ��ˮ�д�������ƽ�⣺![]() ��
��![]() ���ﵽƽ���Ҫʹ
���ﵽƽ���Ҫʹ![]() ��Ũ�����ɼ���������������������
��Ũ�����ɼ���������������������
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪�� ![]() ��Һ�Ǽ���
��Һ�Ǽ���![]() ���Լ�������Һ�д���
���Լ�������Һ�д���![]() ����������ɫ��������
����������ɫ��������![]() ��KI��Һ��
��KI��Һ��![]()
![]() ��Һ�������Ϻ�ȡ���Һ�ֱ��������ʵ�飬��˵����Һ�д��ڻ�ѧƽ�⡰
��Һ�������Ϻ�ȡ���Һ�ֱ��������ʵ�飬��˵����Һ�д��ڻ�ѧƽ�⡰![]() ������
������
ʵ���� | ʵ����� | ʵ������ |
�� | ����KSCN��Һ | ��Һ���ɫ |
�� | ���� | �л�ɫ�������� |
�� | ���� | ����ɫ�������� |
�� | ���������Һ | ��Һ����ɫ |
A. �� B. �ں͢� C. �ۺ͢� D. �ٺ͢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ڸ����������£�����ѡ����ʾ�����ʼ�ת������ʵ�ֵ���(����)
A. NaCl(aq)![]() NaHCO3(s)
NaHCO3(s)![]() Na2CO3(s)
Na2CO3(s)
B. FeS2![]() SO2
SO2![]() H2SO4
H2SO4
C. SiO2![]() SiCl4
SiCl4![]() Si
Si
D. N2![]() NH3
NH3![]() NH4Cl(aq)
NH4Cl(aq)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���õ�ⷨ���ᴿ����ijЩ����������ʵĴ�KOH��Һ���乤��ԭ����ͼ��ʾ�������й�˵���������
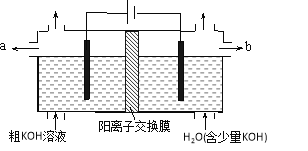
A. ͨ���������������ҺpH������
B. ������ӦʽΪ4OH��-4e����2H2O+O2��
C. ������KOH��Һ��b���ڵ���
D. K+ͨ������Ĥ������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������:Ԫ�ظ�(Cr)����Һ����Ҫ��Cr3+(����ɫ) ��Cr(OH)4-(��ɫ) ��Cr2O72���Ⱥ�ɫ����CrO42����ɫ������ʽ���ڣ�Cr(OH)3Ϊ������ˮ�Ļ���ɫ���壬�ش��������⣺
��1����(24Cr)����________��ѡ���ţ���
a.����Ԫ�� b.����Ԫ�� c.����Ԫ�� d.����Ԫ��
��2��CrO42��Cr2O72����Һ�п��ת���������£���ʼŨ��Ϊ1.0 mol��L1��Na2CrO4��Һ��c��Cr2O72����c��H+���ı仯��ͼ��ʾ��
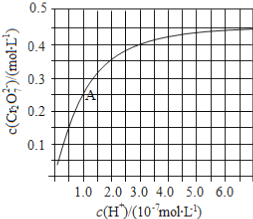
�������ӷ���ʽ��ʾNa2CrO4��Һ�е�ת����Ӧ____________��
����ͼ��֪����Һ��������CrO42��ƽ��ת����__________��������������С��������������������A�����ݣ��������ת����Ӧ��ƽ�ⳣ��Ϊ__________��
�������¶ȣ���Һ��CrO42��ƽ��ת���ʼ�С����÷�Ӧ����H_________0������>����<������=������
��3�������ͷ�ˮ���ؽ���Ԫ�ظ��Ķ��ԣ��ɽ�Cr2O72-ת��ΪCr(OH)3������ȥ����֪��
�������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
Fe2+ | 7.0 | 9.0 |
Fe3+ | 1.9 | 3.2 |
Cr3+ | 6.0 | 8.0 |
ij������ˮ��������Ҫ������ͼ��ʾ��
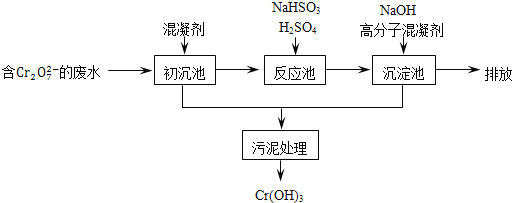
���������м���Ļ�������K2SO4�qAl2(SO4)3�q24H2O��������Ϊ__________�������ӷ���ʽ��ʾ����
����Ӧ������NaHSO3�����Է�Һ�е�Cr2O72-��ԭ��Cr3+���÷�Ӧ�����ӷ���ʽΪ________���������������������кͷ�����ԭ������������м���NaOH��Һ���˹����з�����Ҫ��Ӧ�����ӵ��Ⱥ�˳����____________��֤��Cr3+������ȫ�ķ�����__________��
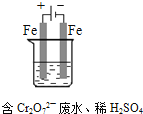
��4����ҵ���õ�ⷨ�������� Cr2O72-��ˮ��ʵ����������ͼģ�����Cr2O72-�ķ�ˮ��������Ӧʽ��Fe-2e-�TFe2+��������Ӧʽ��2H++2e-�TH2����Fe2+��������Һ�е�Cr2O72-��Ӧ�����ӷ���ʽ��__________���õ��Ľ������������������ɳ�����ȫ���õ�ⷨ��������Һ��0.01mol Cr2O72-ʱ�����ٵõ�������������__________ g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����ͼ��ʾʵ�����m gͭ���Ͻ���Ʒ��ͭ������������
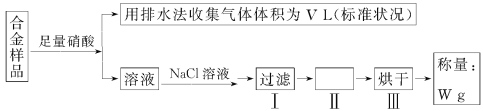
����˵���в���ȷ���� (����)
A. �ռ�����V L����ȫΪNO
B. �����õ��IJ����������ձ���©����������
C. ������Ӧ��ϴ��
D. ͭ����������Ϊ![]() ��100%
��100%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������������ںϳ���ά���ǣ�������
A. �л����� B. ���� C. ��ľ D. ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com