
离子反应为:a![]() +bI-+2nH+→aMn2++cI2+d
+bI-+2nH+→aMn2++cI2+d![]() +nH2O;根据该离子方程式,下列说法正确的是( )
+nH2O;根据该离子方程式,下列说法正确的是( )
A.氧化性![]() <
<![]()
B.c=d=5,则该反应转移电子数为30e-
C.a、b、c、d之间的关系是:5a=2c+6d;b=2c+d
D.当反应物的相对量或浓度发生改变时,化学计量数一定有c=d
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:阅读理解
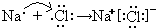
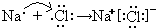
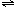 NH3?H2O+H+
NH3?H2O+H+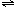 NH3?H2O+H+
NH3?H2O+H+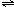 BiOCl+2HCl
BiOCl+2HCl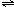 BiOCl+2HCl
BiOCl+2HCl查看答案和解析>>
科目:高中化学 来源: 题型:
A.氧化性![]() <
<![]()
B.c=d=5,则该反应转移电子数为30e-
C.a、b、c、d之间的关系是:5a=2c+6d;b=2c+d
D.当反应物的相对量或浓度发生改变时,化学计量数一定有c=d
查看答案和解析>>
科目:高中化学 来源:新疆自治区月考题 题型:单选题
查看答案和解析>>
科目:高中化学 来源: 题型:
离子反应为aMnO4 - + bI-+x H+→y Mn2++ cI2 + dIO3- + zH2O;根据该离子方程式,下列说法正确的是 ( )
A.氧化性MnO4 ->IO3-
B.c=d=5,则该反应转移电子数为30e
C.该反应的氧化产物只有IO3-
D.a、b、c、d之间的关系是:5a=2c+6d;b=2c+d
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com