
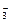 的物质的量浓度之比是1:2,则Cl2与KOH反应时,被还原的氯元素与被氧化的氯元素的物质的量之比是
的物质的量浓度之比是1:2,则Cl2与KOH反应时,被还原的氯元素与被氧化的氯元素的物质的量之比是| A.2:3 | B.4:3 |
| C.10:3 | D.11:3 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:单选题
| A.0.0446 mol·L-1 | B.0.0893 mol·L-1 |
| C.0.1786 mol·L-1 | D.0.0223 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Fe(OH)3 | B.FeCl3 | C.I2 | D.Fe2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.都是3 mol·L-1 |
| B.分别是4 mol·L-1和1 mol-1 |
| C.分别为1 mol·L-1和4 mol·L-1 |
| D.都是6 mol·L-1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.KCl、KBr | B.KCl、I2 |
| C.Br2、I2 | D.KCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.氯气是一种黄绿色、有毒的气体 |
| B.氯元素在自然界中既可以以化合态存在,也可以以游离态存在 |
| C.氯气可用向下排空气法收集 |
| D.氯气、氯水、液氯是同一种物质,只是状态不同,都属于纯净物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com