
【题目】常温下,用0.1 mol/LNaOH溶液滴定10mL 0.1mol/LH2A溶液,溶液的pH与NaOH溶液的体积关系如图所示.下列说法不正确的是( )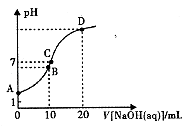
A.A点溶液中加入少量水: ![]() 增大
增大
B.B点:c( HA ﹣)>c(H+)>c(A2-)>c(H2A)
C.C点:c(Na+)=c(HA﹣)+2c( A2﹣)
D.水电离出来的c(OH﹣):B点>D点
【答案】D
【解析】解:A.根据图象可知,0.1mol/L的H2A溶液的pH大于1,说明H2A为弱酸,若A点溶液中加入少量水,溶液中氢离子、H2A的浓度减小,由于水的离子积不变,则氢氧根离子浓度增大,所以 ![]() 的比值增大,故A正确;
的比值增大,故A正确;
B.B点时加入了10mLNaOH溶液,反应后溶质为NaHA,此时溶液的pH小于7,说明HA﹣的电离程度大于其水解程度,则c(A2﹣)>c(H2A),由于氢离子还来自水的电离,则c(H+)>c(A2﹣),溶液中离子浓度大小为:c( HA ﹣)>c(H+)>c(A2﹣)>c(H2A),故B正确;
C.C点溶液的pH=7,为中性溶液,则c(H+)=c(OH﹣),根据电荷守恒c(Na+)+c(H+)=c(HA﹣)+2c( A2﹣)+c(OH﹣)可知:c(Na+)=c(HA﹣)+2c( A2﹣),故C正确;
D.B点反应后溶质为NaHA,HA﹣的电离程度大于其水解程度,溶液呈酸性,氢离子抑制了水的电离,而D点加入20mL氢氧化钠溶液,二者恰好反应生成Na2A,A2﹣水解促进了水的电离,所以水电离的c(OH﹣):B点<D点,故D错误;
故选D.


科目:高中化学 来源: 题型:
【题目】相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去).其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO.
已知:
Ⅰ、 ![]()
Ⅱ、 ![]()
请根据所学知识与本题所给信息回答下列问题:
(1)X的分子中最多有个原子共面.
(2)H的结构简式是 .
(3)反应③、④的类型是; .
(4)反应⑤的化学方程式是 .
(5)![]() 有多种同分异构体,其中含有1个醛基和2个羟基,且核磁共振氢谱显示为6组峰的芳香族化合物共有种.
有多种同分异构体,其中含有1个醛基和2个羟基,且核磁共振氢谱显示为6组峰的芳香族化合物共有种.
(6)请用合成反应流程图表示出由A和其他无机物(溶剂任选)合成 ![]() 最合理的方案. 示例如下:
最合理的方案. 示例如下: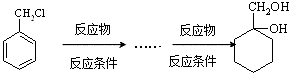
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】聚乙酸乙烯酯广泛用于制备涂料、粘合剂等,它和高聚物K的合成路线如下: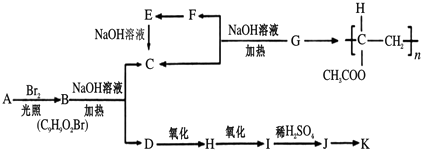
其中J物质与氯化铁溶液能发生显色反应,且苯环上的一元取代物有两种.
已知:
①当羟基与双键碳原子相连时,易发生如下转化RCH=CHOH→RCH2CHO
②一ONa连在烃基上不会被氧化
请回答下列问题:
(1)化合物H中官能团的名称 , 写出G的结构简式 .
(2)上述变化中G→C+F 的反应类型是;J在﹣定条件下能生成高聚物K,K的结构简式是 .
(3)下列有关说法正确的是 . a.1molA 完全燃烧消耗10.5mol O2
b.J与足量的碳酸氢钠溶液反应能生成相应的二钠盐
c.D→H的试剂通常是KMnO4 酸性溶液
d.J能发生加成、消去、取代、氧化等反应
(4)写出B→C+D反应的化学方程式: .
(5)同时符合下列条件的A的同分异构体有种.I.含有苯环 II.能发生银镜反应 III.能发生水解反应.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列操作中,一般情况下不能相互接触的是( )
A. 用胶头滴管向试管内滴加液体时,胶头滴管尖端与试管
B. 分液时,分液漏斗下端与烧杯内壁
C. 过滤时,烧杯内壁与漏斗下端
D. 过滤时,玻璃棒与三层滤纸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神舟”号载人航天器中,宇航员所在的返回舱都是密封的,宇航员吸入氧气,呼出二氧化碳,如果二氧化碳浓度过大,会使宇航员困乏,呼吸频率加快,严重的会窒息,为使二氧化碳浓度降低而保持舱内氧气的适当比例,可以在返回舱内放入( )
A. 过氧化钠B. 碳酸钠C. 氢氧化钠D. 氧气瓶
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂(易被氧化),某研究性学习小组为了制备少Na2S2O5,并探究SO2的某些性质,设计下图所示装置(夹持装置已略去)。请回答下列问题。
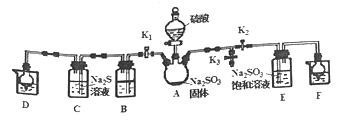
(1)向A中滴加的硫酸最好选用______(填字母)。
A.98%的浓硫酸 B.70%的硫酸 C.10%的稀硫酸
(2)打开分液漏斗旋塞,发现其中的液体不能流下,应采取的操作是___________.
(3)装入药品后,打开K1、K2、K3并从K3处通入一段时间的N2,其目的是______,N2充满装置后再关闭K1、K3,打开K2,滴入硫酸后E中有Na2S2O5晶体析出,装置E中的反应方程式为_____
(4)关闭K2、K3,打开K1,若探究SO2的漂白性,装置B应盛有_____溶液,若B中所装溶液为酸性KMnO4溶液,B中发生反应的离子方程式为______,B中紫色完全褪去后,继续滴加硫酸,则装置C中观察到的现象是__________。
(5)若B中为新制的氯水,将SO2通入其中,请设计简单实验验证二者是否恰好完全反应(简要描述实验步骤、现象和结论)
仪器自选,供选择试剂:滴加酚酞的氢氧化钠溶液、氯化亚铁溶液、硫氰化钾溶液、品红溶液。
___________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种高效水处理剂,某实验小组用下图所示装置制取并收集ClO2 . 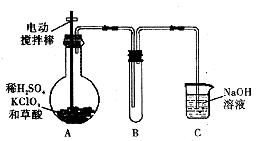
已知:①ClO2为黄绿色气体,极易溶于水,熔点﹣59C,沸点11℃,具有强氧化性.
②ClO2易爆炸,若用“惰性气体”等稀释时,爆炸的可能性大大降低.
③装置A中发生反应:H2C2O4+H2SO4+2KC1O3一K2SO4+2CO2 T+2ClO2+2H2O
④HClO2是强酸.
(1)A装置中电动搅拌棒的作用是 .
(2)B装置需放在冰水中,原因是 .
(3)用H2C2O4、稀硫酸和KClO3制备ClO2的最大优点是 .
(4)ClO2很不稳定,需随用随制,产物用水吸收得到ClO2溶液.为测定所得溶液中ClO2的含量,进行下列实验:步骤1:准确量取V1mL ClO2溶液加入到锥形瓶中.,
步骤2:用稀硫酸调节ClO2溶液的pH≤2.0,加入足量的KI晶体,静置片刻.
步骤3:加入指示剂,用c mol.L﹣1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液V2mL.
(已知2ClO2+8H++10I﹣=2Cl﹣+5I2+4H2O,2S2O32﹣+I2=2I﹣+S4O62﹣)
①配制100mL cmol﹣L﹣lNa2S203标准溶液时,用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管和 .
②原溶液中ClO2的含量为g/L(用含字母的代数式表示).
(5)工业上生产ClO2和NaCIO2的工艺流程如图:
①反应器I中发生反应的化学方程式为 .
②反应器Ⅱ中发生反应的离子方程式为 .
③在碱性溶液中NaClO2比较稳定,所以反应器Ⅱ中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】容量瓶是用来配制物质的量浓度的溶液的定量仪器,其上标有:①温度、②浓度、③容量、④压强、⑤刻度线、⑥酸式或碱式这六项中的 ( )
A. ②④⑥ B. ①③⑤ C. ①②④ D. ③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、d、e、f为六种原子序数依次增大前20号主族元素,a、b、c、d位于同周期,b、f位于同主族,其中a、b、f 为金属元素,c的最外层电子数是其次外层电子数的3倍,c与f 的原子序数和是e的2倍。下列说法错误的是
A. 原子半径a>b>c>d
B. 最简单气态氢化物的稳定性e<c<d
C. 最高价氧化物对应的水化物的碱性f>b
D. fc2、ec2两种化合物中c的化合价相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com