
【题目】合成药物的中间体M合成路线如下:

已知:①RX![]() RCN
RCN
②
请回答:
(1)D![]() E的反应类型是______。
E的反应类型是______。
(2)下列说法不正确的是______。
A.化合物B的官能团有羟基和氯原子
B.1 mol化合物B最多可消耗3 mol NaOH
C.化合物C至少有12个原子在同一平面
D.化合物D能发生加成反应和消去反应
(3)写出E+F![]() M的化学反应方程式: _________________。
M的化学反应方程式: _________________。
(4)写出符合下列条件的C的所有同分异构体: ______。
①分子中除苯环外还含有五元环,是苯环的邻位二取代物
②IR谱显示存在(C—N),且能发生银镜反应
(5)结合题给信息,设计以CH3CH2Cl为原料制备F的合成路线。(用流程图表示,无机物任选)_________________
【答案】 氧化反应 B 
![]() 、
、 、
、![]() 、
、![]() 、
、
![]() 。
。
【解析】本题考查有机物的推断,(1)D的分子式为C12H15NO2,对比D和E的分子式,E比D少了两个氢原子,即D→E发生氧化反应;(2)A、A→B在光照条件下与氯气发生取代反应,氯气取代烷基上的氢原子,根据合成路线以及信息,氯原子取代甲基上的氢原子,即B的结构简式为![]() ,含有的官能团是羟基和氯原子,故A说法正确;B、1molB中含有1mol酚羟基和1mol氯原子,因此最多消耗2molNaOH,故B说法错误;C、根据信息①,C的结构简式为:
,含有的官能团是羟基和氯原子,故A说法正确;B、1molB中含有1mol酚羟基和1mol氯原子,因此最多消耗2molNaOH,故B说法错误;C、根据信息①,C的结构简式为:![]() ,苯环空间构型为平面六边形结构,因此至少有12个原子共面,故C说法正确;D、化合物D中含有苯环和-CN,能与氢气发生加成反应,羟基连接碳原子的相邻的碳原子上有H,能发生消去反应,故D说法正确;(3)E的结构简式为:
,苯环空间构型为平面六边形结构,因此至少有12个原子共面,故C说法正确;D、化合物D中含有苯环和-CN,能与氢气发生加成反应,羟基连接碳原子的相邻的碳原子上有H,能发生消去反应,故D说法正确;(3)E的结构简式为: ,E和F反应的方程式为:
,E和F反应的方程式为: ;(4)除苯环外还有一个五元环,且是邻位的二取代物,IR谱显示存在C-N键,能发生银镜反应,说明含有醛基,因此符合条件的结构简式为:
;(4)除苯环外还有一个五元环,且是邻位的二取代物,IR谱显示存在C-N键,能发生银镜反应,说明含有醛基,因此符合条件的结构简式为:![]() 、
、 、
、![]() 、
、![]() 、
、 ;(5)根据信息①②,CH3CH2Cl应先转化成CH3COOH,即先在NaOH水溶解加热,发生水解或取代反应,生成CH3CH2OH,然后被氧化成CH3COOH,在PCl3作用下生成CH2ClCOOH,最后生成目标产物,即路线图为:
;(5)根据信息①②,CH3CH2Cl应先转化成CH3COOH,即先在NaOH水溶解加热,发生水解或取代反应,生成CH3CH2OH,然后被氧化成CH3COOH,在PCl3作用下生成CH2ClCOOH,最后生成目标产物,即路线图为:![]() 。
。


 习题精选系列答案
习题精选系列答案科目:高中化学 来源: 题型:
【题目】用Na2FeO4溶液氧化废水中的还原性污染物M,为研究降解效果.设计如下对比实验探究温度、浓度、 pH、催化剂对降解速率和效果的影响,实验测得M的浓度与时间关系如图所示,
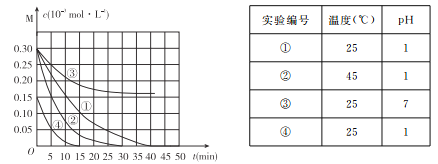
下列说法不正确的是
A. 实验①在15 min内M的降解速率为1.33×10-5mol/(L·min)
B. 若其他条件相同,实验①②说明升高温度,M降解速率增大
C. 若其他条件相同,实验①③证明pH越高,越不利于M的降解
D. 实验④说明M的浓度越小,降解的速率越快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数约为6.02×1023/mol,下列说法一定正确的是( )
A. 60gSiO2晶体中,约含有2×6.02×1023个Si-O键
B. 78gNa2O2晶体中约有2×6.02×1023个阴离子
C. 720g C60晶体约含有6.02×1023个如图中晶胞单元

D. 14g两种烯烃CnH2n和CmH2m混合物,含有共用电子对数目约为3×6.02×1023
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E、F六种元素,A是周期表中原子半径最小的元素,B是电负性最大的元素,C的2p轨道中有三个未成对的单电子,F原子核外电子数是B与C核外电子数之和,D是主族元素且与E同周期,E正一价阳离子M能层电子己排满。D与B可形成离子化合物其晶胞结构如图所示。请回答下列问题:
(1)E元素原子基态时的价电子排布图为___________;
(2)A2F分子中F原子的杂化类型是_______,F的氧化物FO3分子空间构型为______;
(3)CA3极易溶于水,其原因主要是________,试判断CA3溶于水后形成CA3·H2O的合理结构________(填字母代号),从氢键的形成角度回答推理依据是:___________。
(a) (b)
(b)
(4)E的晶胞常采取________堆积方式。
(5)从图中可以看出,D跟B形成的离子化合物的化学式为_________;该离子了化合物晶体的密度为ag/cm3,则晶胞的体积是_______cm3(写出表达式即可,NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应X+Y=M+N为吸热反应,对这个反应的下列说法中正确的是( )
A.X的能量一定低于M的,Y的能量一定低于N的
B.因为该反应为吸热反应,故一定要加热反应才能进行
C.破坏反应物中的化学键所吸收的能量小于形成生成物中化学键所放出的能量
D.X和Y的总能量一定低于M和N的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列氯化物中,既能由金属和氯气直接反应制得,又能由金属和盐酸反应制得的( )
A. CuCl2 B. FeCl2 C. AlCl3 D. FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验需要100mL、0.1mol/L的Na2CO3溶液,现通过如下操作配制:
①把称量好的固体Na2CO3放入小烧杯中,加适量蒸馏水溶解。为加快溶解可以使用________(填仪器名称)搅拌;②把①所得溶液冷却到室温后,小心转入________(填仪器名称);③继续加蒸馏水至液面至刻度线1~2cm处,改用________(填仪器名称)小心滴加蒸馏水至溶液凹液面最低点与刻度线相切;④用少量蒸馏水洗涤玻璃棒和烧杯2~3次,每次洗涤的溶液都小心转入容量瓶,并轻轻摇匀;⑤将容量瓶塞紧,充分摇匀。
(1)操作步骤正确的顺序是________(填序号)。
(2)若没有操作④,则所配溶液的浓度会________(填“偏高”或“偏低”)。
(3)若所配溶液的密度为1.06g/mL,则该溶液的质量分数为________。
(4)若取出20mL配好的Na2CO3溶液,加蒸馏水稀释成c(Na+)=0.01mol/L的溶液,则稀释后溶液的体积为________mL。
(5)在配制100mL、0.1mol/L的Na2CO3溶液时,下列操作中的________会导致结果偏低(请用序号填写)。
a.将烧杯中的溶液转移到容量瓶时不慎洒到容量瓶外
b.定容时俯视刻度线
c.定容时仰视刻度线
d.干净的容量瓶未经干燥就用于配制溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com