
氯化钠是日常生活中人们常用的调味品,下列性质可以证明氯化钠中一定存在离子键的是
| A.具有较高的熔点 | B.熔融状态下能导电 |
| C.水溶液能导电 | D.常温下能溶于水 |
科目:高中化学 来源: 题型:单选题
一种新催化剂,能在室温下催化空气氧化甲醛:HCHO+O2 CO2+H2O,该反应
CO2+H2O,该反应
| A.反应物和生成物中都含极性分子和非极性分子 |
| B.生成1.8gH2O消耗2.24L O2 |
| C.反应时有极性键和非极性键的断裂和它们的生成 |
| D.为吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
硼及其化合物在催化剂制造、储氢材料、燃料电池等方面应用广泛。Li3BN2是一种价格低廉且性能优良的储氢材料,其储氢与放氢原理为Li3BN2+4H2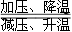 Li3BN2H8。下列有关说法正确的是
Li3BN2H8。下列有关说法正确的是
| A.B的原子半径小于N的原子半径 |
| B.H2的结构式为H—H |
| C.放氢过程为化合反应 |
| D.储氢过程没有能量变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于化学键的叙述正确的是
A.非金属元素组成的化合物中只含共价键
B.C、N、O、H四种元素形成的化合物一定既有离子键,又有共价键。
C.不同元素的原子构成的分子只含极性共价键
D.CH4中所有的价电子都参与形成共价键
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列选项的说法中正确的是
| A.分子的结构是由键角决定的 |
| B.共价键的键能越大,共价键越牢固 |
| C.CF4、CCl4、CBr4、CI4中C—X键的键长、键角均相等 |
| D.H2O分子中的两个O—H键的键角为180° |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
2004年7月德俄两国化学家共同宣布,在高压下氮气会发生聚合得到高聚氮,这种高聚氮的N-N键的键能为160kJ/mol(N2的键能为942kJ/mol),晶体片段结构如图所示。又发现从N2可制取出N5、N3。含N5+离子的化合物及N60、N5极不稳定。则下列说法错误的是:
| A.该晶体中含有非极性共价键 |
| B.含N5+离子的化合物中既有离子键又有共价键 |
| C.高聚氮与N2、N3、N5、N5+、N60互为同素异形体 |
| D.这种固体的可能潜在应用是烈性炸药或高能材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关离子键和离子化合物的说法正确的是( )
| A.凡含离子键的化合物,一定含金属元素 |
| B.在化合物MgCl2中,两个氯离子之间也存在离子键 |
| C.离子化合物一定能导电 |
| D.原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com