
| A. | F? | B. | C1? | C. | NH3 | D. | H2O |
分析 氢氧根离子中质子数为各元素的质子数之和,一个氢氧根离子中的质子数是9个,电子数是10个.
解答 解:氢氧根离子中质子数为各元素的质子数之和,一个氢氧根离子中的质子数是9个,电子数是10个.
A、F-中质子数是9,电子数是10,和氢氧根离子中质子数和电子数都相同,故A正确;
B、Cl-中质子数是17,电子数是18,所以和氢氧根离子中质子数不同,电子数相同,故B错误;
C、NH3分子中质子数是10,电子数是10,所以和氢氧根离子中质子数相同,电子数不同,故C错误;
D、H2O中质子数是10,电子数是10,所以和氢氧根离子中质子数不相同,故D错误.
故选A.
点评 本题考查了离子中质子数和电子数的计算,难度不大,明确阳离子中质子数=电子数+电荷数,阴离子中质子数=电子数-电荷数.


科目:高中化学 来源: 题型:选择题
| A. | 两者产生等量的氢气 | B. | 强酸溶液产生氢气的速度快 | ||
| C. | 弱酸溶液产生较多的氢气 | D. | 无法比较两者产生氢气的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ②③④⑥ | C. | ②③⑥ | D. | ③⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ⑤②①④③ | B. | ⑤①②③④ | C. | ④③②①⑤ | D. | ④③①②⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铂金做首饰不能用金属键理论解释 | |
| B. | 固态和熔融时易导电,熔点在1 000℃左右的晶体可能是金属晶体 | |
| C. | Li、Na、K的熔点逐渐升高 | |
| D. | 金属导电和熔融电解质(或电解质溶液)导电的原理一样 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X一定是碱金属元素 | |
| B. | Y元素能形成化合物Na2YO3,且其水溶液呈碱性 | |
| C. | Z元素形成的最高价氧化物熔点较低 | |
| D. | X的单质一定能通过电解Z的盐酸盐溶液制备 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
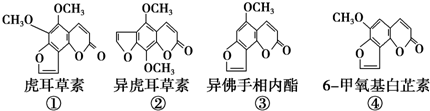
| A. | ①与②、③与④分别互为同分异构体 | |
| B. | 等物质的量的②、④分别在足量氧气中完全燃烧,前者消耗氧气比后者多 | |
| C. | ①、②、③、④均能与氢氧化钠溶液反应 | |
| D. | ①、④互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com