
【题目】甲烷重整可以获得CO、H2等重要化工原料,相关反应原理如下: ①CH4(g)+ ![]() O2(g)CO(g)+2H2(g)△H=﹣36kJ/mol
O2(g)CO(g)+2H2(g)△H=﹣36kJ/mol
②CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206kJ/mol
③CH4(g)+CO2(g)2CO(g)+2H2(g)△H=+247kJ/mol副反应
④CH4(g)+2O2(g)CO2(g)+2H2O (g)△H=﹣889.6kJ/mol
(1)反应CO2 (g)+H2(g)CO (g)+H2O(g)△H= .
(2)某温度下,向体积为1L的密闭容器中充入1molCH4和1molCO2 , 只发生反应③,测得CH4(g)和CO(g)的浓度随时间变化曲线如图(1)所示.计算0~5小时H2的平均反应速率 , 该温度下的平衡常数为(保留两位有效数字),若再往容器中充0.4molCH4和0.2molCO,其它条件不变,则平衡向方向移动.
(3)研究人员研究混合气体比例对重整气CO和H2含量影响,在初始温度为973K时,n(O2)/n(H2O)按不同比例投入不同反应容器(绝热)重整相同的时间,重整的数据如图(2):从图可知,重整气CO的含量随 ![]() 增大而增大,其主要原因是 .
增大而增大,其主要原因是 .
(4)甲烷重整可选氧化物NiO﹣Al2O3作为催化剂.工业上常用Ni(NO3)2、Al(NO3)3混合液加入氨水调节pH=12(常温),然后将浊液高压恒温放置及煅烧等操作制备.加入氨水调节pH=12时,c(Ni2+)为 . 已知:Ksp[Ni(OH)2]=5×10﹣16 .
【答案】
(1)41kJ/mol
(2)0.12mol/(L?h);1.1(mol/L)2;正
(3)反应②③是吸热反应,反应①④是放热反应,增加n(O2)/n(H2O),①④将向正方向移动,反应产生的热量促使反应②③向正方向移动
(4)5×10﹣12mol/L
【解析】解:(1)已知①CH4(g)+ ![]() O2(g)CO(g)+2H2(g)△H=﹣36kJ/mol②CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206kJ/mol③CH4(g)+CO2(g)2CO(g)+2H2(g)△H=+247kJ/mol副反应④CH4(g)+2O2(g)CO2(g)+2H2O (g)△H=﹣889.6kJ/mol据盖斯定律,反应[(①﹣②)×4+(③﹣④)]÷2得
O2(g)CO(g)+2H2(g)△H=﹣36kJ/mol②CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206kJ/mol③CH4(g)+CO2(g)2CO(g)+2H2(g)△H=+247kJ/mol副反应④CH4(g)+2O2(g)CO2(g)+2H2O (g)△H=﹣889.6kJ/mol据盖斯定律,反应[(①﹣②)×4+(③﹣④)]÷2得 ![]() =41KJ/mol,所以答案是:41kJ/mol;(2)0~5小时时CO的浓度从0变化到0.60mol/L,据化学方程式可知,氢气的反应速率v(H2)=
=41KJ/mol,所以答案是:41kJ/mol;(2)0~5小时时CO的浓度从0变化到0.60mol/L,据化学方程式可知,氢气的反应速率v(H2)= ![]() =0.12mol/(Lh);
=0.12mol/(Lh);
平衡时浓度[CO]=[H2]=0.8mol/L,[CO2]=[CH4]=0.60mol/L,化学平衡常数K= ![]() =
= ![]() =1.1;再往容器中充0.4molCH4和0.2molCO,容器体积为1L,Qc=
=1.1;再往容器中充0.4molCH4和0.2molCO,容器体积为1L,Qc= ![]() =1.07<1.1,平衡正向移动,所以答案是:0.12mol/(Lh);1.1(mol/L)2;正;(3)反应①CH4(g)+
=1.07<1.1,平衡正向移动,所以答案是:0.12mol/(Lh);1.1(mol/L)2;正;(3)反应①CH4(g)+ ![]() O2(g)CO(g)+2H2(g)△H=﹣36kJ/mol
O2(g)CO(g)+2H2(g)△H=﹣36kJ/mol
②CH4(g)+H2O(g)CO(g)+3H2(g)△H=+206kJ/mol
③CH4(g)+CO2(g)2CO(g)+2H2(g)△H=+247kJ/mol副反应
④CH4(g)+2O2(g)CO2(g)+2H2O (g)△H=﹣889.6kJ/mol
中,反应②③是吸热反应,反应①④是放热反应,增加n(O2)/n(H2O),①④将向正方向移动,反应产生的热量促使反应②③向正方向移动,
所以答案是:反应②③是吸热反应,反应①④是放热反应,增加n(O2)/n(H2O),①④将向正方向移动,反应产生的热量促使反应②③向正方向移动;(4)pH=12,c(OH﹣)=0.01mol/L,Ksp[Ni(OH)2]=5×10﹣16 , c(Ni2+)= ![]() =5×10﹣12mol/L,所以答案是:5×10﹣12mol/L.
=5×10﹣12mol/L,所以答案是:5×10﹣12mol/L.
【考点精析】解答此题的关键在于理解反应热和焓变的相关知识,掌握在化学反应中放出或吸收的热量,通常叫反应热,以及对化学平衡的计算的理解,了解反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%.


 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案科目:高中化学 来源: 题型:
【题目】硅旧称矽,矽病是一种职业病,采矿、翻砂、喷砂、制陶瓷、制耐火材料等场所工作的人易患此病。因此,在这些粉尘较多的工作场所,应采取严格的劳动保护措施,采用多种技术和设备控制工作场所的粉尘含量,以保证工作人员的身体健康。你认为引起硅肺病的主要原因是粉尘中大量含有
A.二氧化硅B.硅C.硅酸D.硅酸盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室制取并收集氯气的装置图.请回答下列问题: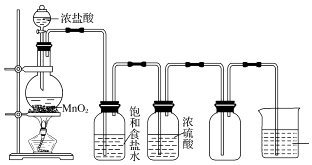
(1)实验室制取氯气的化学方程式为 .
(2)烧杯中盛放的液体是 , 其作用是 .
(3)8.7g MnO2与足量的浓盐酸充分反应,则被氧化的HCl的物质的量为 , 生成的氯气在标准状况下的体积为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室配制250mL0.1mol/L的盐酸溶液,填空并请回答下列问题:
(1)配制250mL0.1mol/L的盐酸溶液需要mL容量瓶.还需要 , , . (仪器)
(2)配制时,其正确的操作顺序是计算称量溶解 转移定容摇匀装瓶.
(3)若出现如下情况,对所配溶液浓度将有何影响?加蒸馏水时不慎超过了刻度;定容时俯视未冷却 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A.所有含氢元素的化合物中都存在氢键,氢键是一种类似于共价键的化学键
B.离子键、氢键、范德华力本质上都是静电作用
C.只有电负性很强、半径很小的原子(如F、O、N)才能形成氢键
D.氢键是一种分子间作用力,氢键比范德华力强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甘醇可用作溶剂、纺织助剂等,一旦进入人体会导致急性肾衰竭,危及生命。二甘醇的结构简式是HO-CH2CH2-O-CH2CH2-OH。下列有关二甘醇的叙述,正确的是( )
A.符合通式CnH2nO3
B.分子间能形成氢键
C.分子间不存在范德华力
D.能溶于水,不溶于乙醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有下列电子排布式的原子中,半径最大的是( )
A.1s22s22p63s23p1B.1s22s22p3C.1s22s22p2D.1s22s22p63s23p4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com