
环氧树脂具有极强的粘结性,俗称“万能胶”。双酚A是制备环氧树脂的重要原料,其结构为![]() 。下列有关双酚A的叙述不正确的是
。下列有关双酚A的叙述不正确的是
A.能和NaOH溶液反应 B.能和FeCl3溶液反应显紫色
C.能和浓溴水反应 D.苯环上一溴代物有四种
科目:高中化学 来源: 题型:阅读理解
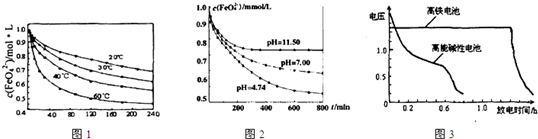
查看答案和解析>>
科目:高中化学 来源: 题型:
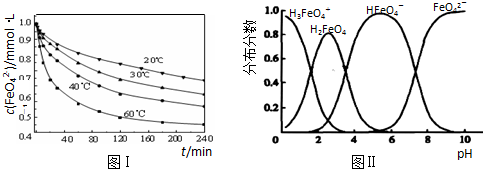
| 放电 | 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+).c(FeO42-) |
| c(HFeO4-) |
| c(H+).c(FeO42-) |
| c(HFeO4-) |
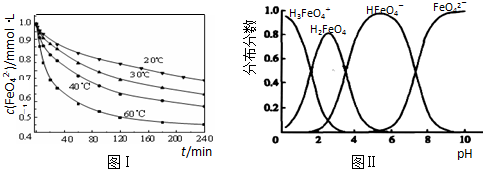
查看答案和解析>>
科目:高中化学 来源: 题型:
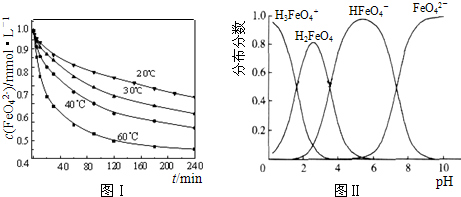
| c(H+).c(FeO42-) |
| c(HFeO4-) |
| c(H+).c(FeO42-) |
| c(HFeO4-) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com