
【题目】下列各物质中,不能发生水解反应的是 ( )
A. 葡萄糖 B. 油脂 C. 蔗糖 D. 蛋白质
科目:高中化学 来源: 题型:
【题目】25℃时,下列不能说明醋酸是弱酸的是
A. 0.1mol/L的醋酸溶液pH>1B. 醋酸钠溶液pH>7
C. 稀醋酸溶液导电能力弱D. 醋酸溶液中含有CH3COOH分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定放置己久的小苏打样品中纯碱的质量分数,设计如下实验方案:
(1)方案一:称取一定质量的样品,罝于坩埚中加热至恒重后,冷却,称取剩余固体质量,计算。实验中加热至恒重的目的是__________________。
(2)方案二:按下图装置进行实验,并回答以下问题。
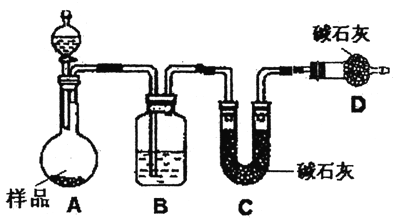
①实验前先____________。分液漏斗中应该装稀_______ (盐酸或硫酸)。D装置的作用是____________。
②实验中除称量样品质量外,还需称_____装置前后质量的变化(填装置的字母代好)。
③根据此实验得到的数据,测定结果有误差。因为实验装置还存在一个明显缺陷,该缺陷是___________。
(3)方案三:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氯化钡溶液。过滤、洗涤,干燥沉淀,称量固体质量,计算。
①采用该方法判断沉淀是否完全的方法是_______________。
②如加入试剂改为氢氧化钡,已知称得样品9. 5g,干燥的沉淀质量为19. 7g,则样品中碳酸钠的质量分数为_______________ (计算结果保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.92g铜投入一定量的浓HNO3中,铜完全溶解,生成的气体颜色越来越浅,共收集到672mL气体(标况).将盛有此气体的容器倒扣在水中,通入标况下一定体积的O2 , 恰好使气体完全溶于水中转变为硝酸,则通入O2的体积(标况)为( )
A.504mL
B.168mL
C.336mL
D.224mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂对工业污泥中的Cr元素回收与再利用的工艺如下(己知硫酸浸取液中的金属离子主要是Cr3+,其次是少量的Fe2+、Fe3+、Al3+、Ca2+、Mg2+):

部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表:
阳离子 | Fe3* | Fe2+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时 的pH | 1.9 | 7.0 | — | 一 | — |
沉淀完全时 的pH | 3.2 | 9.0 | 11.1 | 8 | 9 (>9溶解) |
(1)实验室用98% (密度为1.84 g·cm-3)的浓硫酸配制200mL4.8 mol·L-1的硫酸溶液,配制时需要量取98%的浓硫酸的体积为_________mL (保留小数点后一位小数),所用的玻璃仪器除烧杯、玻璃棒、量筒外,还需__________________________________。
(2)在上述配制稀硫酸过程中,会导致所配溶液浓度偏小的操作是____________________(填序号)
a.定容时俯视刻度线 b.量取浓硫酸时,俯视刻度线
c.当容置瓶中液体占容积2/3左右时,未振荡摇匀 d.转移溶液时,没有等溶液冷却至室温
(3)加入H2O2的作用一方面是氧化+3价Cr使之转变成+6价Cr (CrO42-或Cr2O72-),以便于与杂质离子分离;另一方面是_____________________________。(离子方程式表示)
(4)调节溶液的pH=8除去的杂质离子是___________________。
(5)钠离子交换树脂的原理为:Mn++nNaR→MRn +nNa+,被交换的杂质离子是_____________________。
(6)通SO2气体时,还原过程发生以下反应(填写缺项物质并配平)
____________________________________________________________Na2SO4.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)在①NaCl、②NaOH、③N2、④H2S、⑤Na2O2中,只含有离子键的是 , 只含有极性键的是 , 既含离子键又含非极性共价键的是 .
(2)写出下列物质的结构式:CO2N2HClO .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组以甲苯为主要原料,采用以下路线合成医药中间体F和Y。
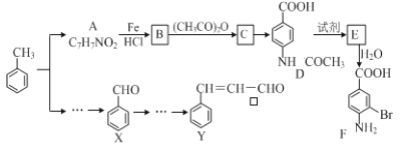
已知:①![]()
![]()
![]()
②![]()
③CH3COOH+CH3COOH→(CH3CO)2O+H2O
请回答下列问题:
(1)下列有关F的说法正确的是______________。
A.分子式是C7H7NO2Br B.F即能与HCl又能与NaOH应生成盐
C.能发生取代反应和缩聚反应 D.1 mol的 F最多可以和2 mol NaOH反应
(2)C→ D的反应类型是 _____。
(3)在合成F的过程中,B→C步骤不能省略,理由是_____________________。
(4)D→E反应所需的试剂是 ___________________。
(5)写出同时符合下列条件的A的同分异构体的结构简式(写出其中1个)_________________。
①苯环上只有两种不同化学环境的氢原子②分子中含有-CHO
(6)利用已知信息,以X和乙烯为原料可合成Y,请设计合成路线(无机试剂及溶剂任选)。___________ 注:合成路线的书写格式参照如下示例流程图:
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】加热N2O5依次发生的分解反应为:
①N2O5(g)![]() N2O3(g)+O2(g)
N2O3(g)+O2(g)
②N2O3(g)![]() N2O(g)+O2(g)
N2O(g)+O2(g)
在容积为2L的密闭容器中充入8molN2O5,加热到t℃,达到平衡状态后O2为9mol,N2O3为3.4mol.则t℃时反应①的平衡常数为
A. 8.5 B. 9.6 C. 10.2 D. 10.7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com