
我国在丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是海水综合利用的一个方面:根据下述流程图,请回答:
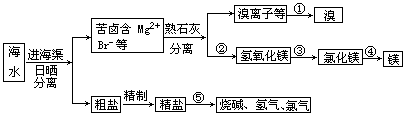
(1)①②两步加入的试剂和有关的离子方程式:______________。
(2)写出③④⑤的化学方程式:______。
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
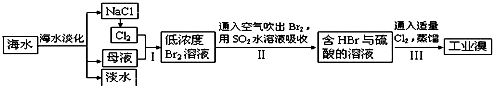
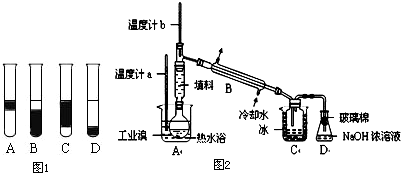
查看答案和解析>>
科目:高中化学 来源: 题型:
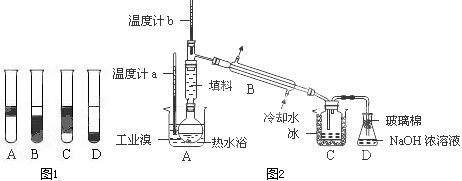
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
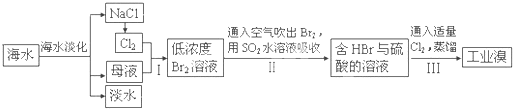
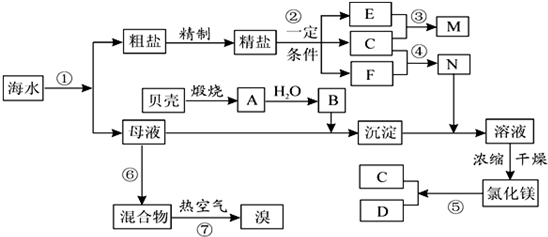
我国有丰富的海水资源,开发和利用海水资源是当前科学研究的一项重要任务,下图是海水综合利用的一个方面。
请回答下列问题:
1、①步主要反应的的离子方程式: 。
溴的用途有很多,写出其中的一种 。
2、分离出氢氧化镁的操作称为 ,第③步需要加入 ,写出该物质在水中的电离方程式: 。
3、将粗食盐中含有的Mg2+、Ca2+和SO42—等杂质除去,加入的试剂有(按加入顺序填入) 。
4、④产物氢气在 极生成,若电解食盐水时消耗NaCl的质量为234g,则在理论上最多可得氯气的体积为___ _升(标准状况)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com