
(9分)某纯碱样品中含有少量氯化钠杂质,现用下图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去)。实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为85.4g;
③准确称得6g纯碱样品放入容器b中;
④打开分液漏斗a的旋塞,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤打开弹簧夹,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为87.6g。试回答:
(1)若④⑤两步的实验操作太快,则会导致测定结果 _ _(填“偏大”或“偏小”);
(2)鼓入空气的目的是______________________,装置A中试剂X应选用_ _;
(3)若没有C装置,则会导致测定结果_____(填“偏大”或“偏小”);
(4)E装置的作用是___________________________________;
(5)装置B中发生反应的离子方程式 ;
(6)根据实验中测得的有关数据,计算出纯碱样品Na2CO3的质量分数为______(计算结果保留一位小数)。

(1)偏小;(2)将装置内残留的CO2气体完全排出,达到精确测量的目的。NaOH溶液;(3)偏大;(4)防止空气中的二氧化碳和水蒸气进入D的干燥管。(5)CO32-+2H+ =CO2↑+H2O;(6)88.3%
【解析】
试题分析:(1)反应过快会使产生的气体二氧化碳没能完全被D装置中碱石灰吸收;快速鼓入空气,也会使装置内残留二氧化碳不能被D装置中碱石灰完全吸收;二氧化碳质量偏小,则测定结果偏小;故答案为:偏小;(2)鼓入空气,可把残留在装置B、C中二氧化碳全部由D中碱石灰吸收;故答案为:使B中产生的二氧化碳全部进入D中因为空气中含有二氧化碳,因此应把鼓入的空气中的二氧化碳吸收处理,所以装置A应放入氢氧化钠溶液或其它碱溶液;故答案为:NaOH溶液或碱性溶液;(3)C装置中的浓硫酸具有吸水性,在装置中吸收由B装置排出气体中混有的水分,若少了此装置则会使气体中的水分被D装置中碱石灰吸收,而使测定质量偏大;故答案为:偏大;(4)如果D装置直接与外界空气相连通,则空气中的水和二氧化碳会对测定结果带来影响,所以装置E的作用则是防止空气中水和二氧化碳进入装置D中;故答案为:防止空气中CO2和水蒸气进入D中;(5)B中离子方程式为CO32- + 2 H+ = CO2 ↑ + H2O;(6)反应中放出二氧化碳气体的质量=85.6g-83.4g=2.2g,设放出2.2g二氧化碳消耗碳酸钠的质量为x,由Na2CO3~CO2关系可知碳酸钠与二氧化碳的物质的量相等,即106:44=x:2.2g 解之得 x=5.3g纯碱样品Na2CO3的质量分数=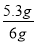 ×100%≈88.3%
×100%≈88.3%
考点:有关化学方程式的计算


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014-2015学年湖南省高三上学期12月联考化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.钾原子结构示意图:
B.水的电子式:
C.CO2的比例模型:
D.间羟基苯甲酸的结构简式:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年甘肃省天水市高三一轮复习基础知识检测化学试卷(解析版) 题型:选择题
化学方程式可简明地体现元素及其化合物的性质。已知:
氧化还原反应:2FeCl3+2HI=2FeCl2+I2+2HCl;2Co(OH)3+6HCl =2CoCl2+Cl2↑+6H2O
2Fe(OH)2+ I2+2KOH = 2Fe(OH)3+2KI; 3I2+6KOH=5KI+KIO3+3H2O
复分解反应:2HSCN +K2CO3 = 2KSCN + CO2 ↑ + H2O;
KCN + CO2 + H2O = HCN + KHCO3
热分解反应:4NaClO 3NaCl + NaClO4;NaClO4
3NaCl + NaClO4;NaClO4 NaCl + 2O2↑
NaCl + 2O2↑
下列说法不正确是
A.氧化性(酸性溶液):FeCl3 > Co(OH)3 > I2
B.还原性(碱性溶液):Fe(OH)2 > I2 > KIO3
C.热稳定性:NaCl > NaClO4 > NaClO
D.酸性(水溶液):HSCN > H2CO3 > HCN
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省襄阳市四校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列各组离子在无色水溶液中能大量共存的是
A.Na+ Mg2+ Cl- OH- B.MnO4- HCO3- OH- K+
C.Fe3+ H+ SO42- CH3COO- D.K+ NO3- CO32- Na+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省襄阳市四校高一上学期期中联考化学试卷(解析版) 题型:选择题
下列生活中的现象与氧化还原反应知识有关的是
A.食盐放在水中片刻后消失了
B.食醋洒在大理石台面上产生气泡
C.烧菜用过的铁锅,放置后常出现红棕色斑迹
D.用食醋可以除去水壶中的水垢[水垢的主要成分为CaCO3、Mg(OH)2]
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一上学期期中化学试卷(解析版) 题型:选择题
锌与很稀的硝酸反应生成硝酸锌、硝酸铵和水。当生成a mol硝酸锌时,被还原的硝酸的物质的量为
A.a mol B.1/2a mol C.1/4a mol D.2a mol
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省松原市高一上学期期中化学试卷(解析版) 题型:选择题
已知 2Fe3+ +2I-=2Fe2+ +I2 2Fe2+ +Cl2 =2Fe3+ +2Cl-
则有关离子的还原性由强到弱的顺序为
A.Cl->Fe2+>I- B.I->Fe2+>Cl-
C.Fe2+>I->Cl- D.Fe2+>Cl->I-
查看答案和解析>>
科目:高中化学 来源:2014-2015吉林省吉林市高一上学期期末考试化学试卷(解析版) 题型:填空题
(10分)
(1)在Cl2、NO、SO2、NO2、NH3五种气体中,与空气相遇立即变色的是 ,常用于自来水杀菌、消毒的是 ,能用向下排空气法收集的是 ,溶于水后能生成强酸的是 。
(2)二氧化氯(ClO2)是目前国际上公认的第四代高效、无毒消毒剂。
①工业上通过下列方法制取ClO2,完成该反应的化学方程式:2KClO3 + SO2 =2C1O2+
②配平下列化学方程式:KClO3+ H2C2O4+ H2SO4= ClO2↑+ K2SO4+ CO2↑+ H2O
下列有关上述反应的说法正确的是 。
A.H2C2O4在反应中被还原 B.KClO3是氧化剂
C.ClO2是还原剂 D.生成1molClO2有2mol电子转移
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省长沙市望城区高一上学期期末化学试卷(解析版) 题型:选择题
下列微粒既有氧化性又有还原性的是
A.H+ B.Cu2+ C.Fe2+ D.Al
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com