
溶液、胶体和浊液这三种分散系的根本区别是( )
A.是否是大量分子或离子的集合体
B.分散质粒子的大小
C.是否能通过滤纸
D.是否均一、透明、稳定
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
如图所示是实验中常用的几种仪器
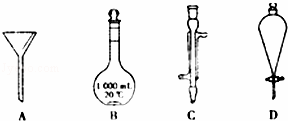
(1)写出序号所代表的仪器的名称A ;B 1 ;C ;D .
(2)上述仪器A~D使用前需要检漏的有 ;不能用于分离的有 .
查看答案和解析>>
科目:高中化学 来源: 题型:
少量铁粉与100mL 0.01mol/L的稀盐酸反应,反应速率太慢.为了加快此反应速率可以使用如下方法( )
A. 加H2O B. 加入饱和食盐水
C. 增大压强 D. 升高温度(不考虑盐酸挥发)
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应X(g)+Y(g)⇌R(g)+Q(g)的平衡常数与温度的关系如表.830℃时,向一个2 L的密闭容器中充入0.2 mol X和0.8 mol Y,反应初始4 s内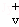 (X)=0.005mol/(L•s).下列说法正确的是( )
(X)=0.005mol/(L•s).下列说法正确的是( )
温度/℃ 700 800 830 1000 1200
平衡常数 1.7 1.1 1.0 0.6 0.4
A. 4 s时容器内c(Y)=0.76 mol/L
B. 830℃达平衡时,X的转化率为80%
C. 反应达平衡后,升高温度,平衡正向移动
D. 1200℃时反应R(g)+Q(g)⇌X(g)+Y(g)的平衡常数K=0.4
查看答案和解析>>
科目:高中化学 来源: 题型:
氨气是重要的化工原料.实验室可用浓氨水和 来制取氨气.
a.烧碱 b.生石灰 c.氯化铵
(2)某实验小组设计了下列装置进行氨的催化氧化实验.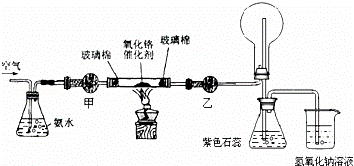
①盛放氨水的实验仪器的名称为 ;在加热条件下,硬质玻璃管中发生反应的化学方程式为 .
②实验时发现:如果缺少乙处的干燥管,将反应后的气体直接通入烧瓶,则烧瓶中先产生白雾,随即产生白烟,其原因是 .
③烧杯中盛有NaOH溶液的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列化学反应的离子方程式正确的是( )
A.氢氧化钡溶液与稀硫酸的反应:OH﹣+H+=H2O
B.澄清的石灰水与稀醋酸反应:Ca(OH)2+2H+=Ca2++2H2O
C.在Ca(HCO3)2溶液中加入过量氢氧化钠溶液:Ca2++HCO3﹣+OH﹣=CaCO3↓+H2O
D.往澄清石灰水通入过量二氧化碳气体:CO2+OH﹣=HCO3﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
从下列事实所得出的相应结论正确的是( )
| 实验事实 | 结论 | |
| ① | Cl2的水溶液可以导电 | Cl2是电解质 |
| ② | 将燃烧的镁条放入CO2中能继续燃烧 | 还原性:Mg>C |
| ③ | 常温下白磷可自燃而氮气须在放电时才与氧气反应 | 非金属性:P>N |
| ④ | 某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 | 该溶液一定有NH4+ |
|
| A. | ③④ | B. | ②④ | C. | ①② | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示的原电池装置
(1)金属Zn组成的电极是 极,发生 反应,电极反应方程式为 ;
(2)金属Cu电极反应方程式为 .
(3)当导线上通过3.01×1022个电子时,锌片质量减少 g,铜片表面析出氢气 L(标准状况).

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com