
【题目】糖类、脂肪和蛋白质是维持人体生命活动所需的三大营养物质。以下叙述正确的是( )
A.植物油不能使溴的四氯化碳溶液褪色B.淀粉水解的最终产物是葡萄糖
C.葡萄糖能发生氧化反应和水解反应D.蚕丝、羊毛、棉花的主要成分都是蛋白质
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A. 25℃ 时,1LpH=1的H2SO4溶液中含有0.1NAH+
B. 常温常压下,18gD2O含有的质子数为10NA
C. 9.0g淀粉和葡萄糖的混合物中共含有0.3NA碳原子
D. 铜粉与硫粉混合加热,每消耗1mol铜粉,转移的电子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下, [已知N2(g)+3H2(g)![]() 2NH3(g) △H=-92.4kJ·mol-1]
2NH3(g) △H=-92.4kJ·mol-1]
容器 | 甲 | 乙 | 丙 |
反应物投入量 | lmolN2 、3molH2 | 2mol NH3 | 4mol NH3 |
NH3的浓度(mol/L) | cl | c2 | c3 |
反应的能量变化 | 放出akJ | 吸收bkJ | 吸收ckJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | a1 | a2 | a3 |
下列说法正确的是
A. a1+a3<1 B. a+b>92.4 C. 2p2<p3 D. 2c1>c3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变a1mol/L元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数δ(X)随pH的变化如图所示,已知[δ(X)= ![]() ]。
]。
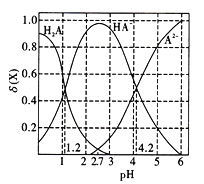
下列叙述错误的是
A. lg[K2(H2A)]=-4.2;pH=2.7时,c(HA-)>c(H2A)=c(A2-)
B. pH=4.2时,c(HA-)=c(A2-)>c(H+);随着pH的升高,c(HA-)/c(H2A)的比值先增大后减小
C. 0.1mol/L的NaHA溶液中存在:c(Na+)+c(A2-)+c(H2A)+c(HA-)=0.2mol/L
D. pH=1.2时,c(H2A)=c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,继通过食盐补碘在全国范围内基本实现消除碘缺乏病目标之后,我国又将启动一项涉及千家万户营MgSO4养健康问题的“补铁工程”.卫生部已批准以酱油为食物载体,逐步开展补铁工程.这里的碘、铁指的是( )
A.元素
B.原子
C.分子
D.单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,甲、乙两容器分别盛有甲烷气体和氨气,已知它们所含原子个数相同,则甲、乙两容器的体积比为( )
A.4:5
B.5:4
C.4:3
D.1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,与盐的水解无关的正确说法是( )
①明矾可以做净水剂;
②实验室配制FeCl3溶液时,往往在FeCl3溶液中加入少量的盐酸;
③用NaHCO3和Al2(SO4)3两种溶液可作泡沫灭火剂;
④在NH4Cl溶液中加入金属镁会产生氢气;
⑤草木灰与铵态氮肥不能混合施用;
⑥比较NH4Cl和Na2S等某些盐溶液的酸碱性.
A. ①④⑥ B. ②③⑤ C. ③④⑤ D. 全有关
【答案】D
【解析】①明矾水溶液中,铝离子可水解生成具有吸附性的氢氧化铝胶体,可用作净水剂,故①正确;
②FeCl3溶液中铁离子水解显酸性,加入盐酸可抑制水解,配制FeCl3溶液时,往往在FeCl3溶液中加入少量的盐酸,故②正确;③泡沫灭火剂的灭火原理为NaHCO3和Al2(SO4)3溶液混合发生双水解反应生成氢氧化铝沉淀和二氧化碳,故③正确;④NH4Cl溶液中铵根离子水解显酸性,NH4Cl+H2ONH3H2O+HCl,加入镁,与盐酸发生反应生成氢气,故④正确;⑤铵根离子和草木灰中的碳酸根离子发生双水解,肥效损耗,草木灰与氨态氮肥不能混合施用,故⑤正确;⑥强酸弱碱盐水解呈酸性,强碱弱酸盐呈碱性,则比较NH4Cl和Na2S等某些盐溶液的酸碱性,是利用盐溶液水解后酸碱性不同,故⑥正确。故选D。
【题型】单选题
【结束】
15
【题目】化工生产中常用MnS作沉淀剂除去Ksp工业废水中的Cu2+:Cu2+(aq)+MnS(s)![]() CuS(s)+Mn2+(aq),下列说法错误的是( )
CuS(s)+Mn2+(aq),下列说法错误的是( )
A. MnS的Ksp比CuS的Ksp大
B. 该反应达到平衡时c(Mn2+)=c(Cu2+)
C. 往平衡体系中加入少量CuSO4固体后,C(Mn2+)变大
D. 该反应的平衡常数![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,在10mL浓度均为0.1mol/LNaOH和NH3H2O混合溶液中,滴加0.1mol/L的盐酸,下列有关溶液中粒子浓度关系正确的是( )
A. 未加盐酸时:c(OH-)>c(Na+)= c(NH3H2O)
B. 加入10mL盐酸时:c(NH4+)+c(H+)=c(OH-)
C. 加入盐酸至溶液pH=7时:c(Cl-) = c(Na+)
D. 加入20mL盐酸时:c(Cl-)=c(NH4+)+c(Na+)
【答案】B
【解析】试题分析:A、在氢氧化钠和氨水的混合溶液中,氢氧化钠电离出等浓度的氢氧根离子和钠离子,氨水也电离出氢氧根离子,所以氢氧根离子浓度大于钠离子浓度,但一水合氨的浓度小于钠离子浓度,错误,不选A;B、加入10毫升盐酸,与氢氧化钠反应恰好生成氯化钠和水,钠离子浓度与氯离子浓度相等,根据电荷守恒可知,c(NH4+) +c(H+)+ c(Na+)=c(OH-) + c(Cl-) ,推出c(NH4+) +c(H+) =c(OH-),正确,选B;C、当溶液为中性,根据电荷守恒可以推出c(NH4+) + c(Na+)=c(Cl-),错误,不选C;D、当加入20毫升盐酸时溶液为氯化钠和氯化铵,显酸性,c(H+)>c(OH-)根据电荷守恒c(NH4+) +c(H+)+ c(Na+)=c(OH-) + c(Cl-)可知c(Cl-) >c(NH4+) +c(Na+),错误,不选D。
考点:溶液中的离子浓度的大小比较
【名师点睛】溶液中的离子浓度大小比较时,需要考虑电解质的电离和水解情况,有时候需要根据电荷守恒或物料守恒进行分析。物料守恒是指电解质溶液中由于电离或水解因素,离子会发生变化变成其它离子或分子等,但离子或分子中某种特定元素的原子的总数是不会改变的。电荷守恒指电解质溶液中所有阳离子所带有的正电荷数与所有的阴离子所带的负电荷数相等。
【题型】单选题
【结束】
21
【题目】含等物质的量NaOH的溶液分别用pH为2和3的CH3COOH溶液中和,设消耗CH3COOH溶液的体积依次为![]() ,则两者的关系正确的是( )
,则两者的关系正确的是( )
A. ![]() B.
B. ![]()
C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将二氧化碳转化为乙烯的装置如图所示,使用的电极材料均为惰性电极。下列说法正确的是( )
A. a为电源的正极 B. 每生成0.1mol乙烯,同时生成6.72LO2
C. 阴极反应式为2CO2+12H++12e-=C2H4+4H2O D. 电解过程中,阳极区溶液中c(H+)逐渐减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com