
【题目】已知有以下物质的相互转化:

试回答:
(1)B的化学式为_____;D的化学式为_____。
(2)写出由E转变成F的化学方程式:______。
(3)常用____(填试剂名称)检验G中的阳离子,其现象为______。
(4)向G溶液中加入A的有关反应的离子方程式为________。
【答案】FeCl2 KCl 4Fe(OH)2+2H2O+O2=4Fe(OH)3 KSCN溶液 棕黄色溶液变为红色溶液 2Fe3++Fe=3Fe2+
【解析】
白色沉淀在空气中变为红褐色沉淀,可确定白色沉淀E为氢氧化亚铁,红褐色沉淀F为氢氧化铁,G为氯化铁;A与盐酸和G溶液均能生产B溶液,则A为铁,B为氯化亚铁;溶液焰色反应呈紫色,则溶液中含有K元素,则D为氯化钾,C为氢氧化钾;
(1)分析可知,B、D分别为氯化亚铁、氯化钾,其化学式分别为:FeCl2;KCl;
(2)氢氧化亚铁变为氢氧化铁的方程式为:4Fe(OH)2+2H2O+O2=4Fe(OH)3;
(3)常用硫氰化钾检验铁离子的存在,硫氰根离子遇到铁离子溶液显血红色;
(4)铁离子与铁反应生成亚铁离子,离子方程式为2Fe3++Fe=3Fe2+;


 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案科目:高中化学 来源: 题型:
【题目】已知X(g)+3Y (g)![]() 2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g) 与1mol Y (g),下列说法正确的是
2W(g) +M (g) △H=-a kJ·mol-1(a>0)。一定温度下,在体积恒定的密闭容器中,加入1 mol X(g) 与1mol Y (g),下列说法正确的是
A. 充分反应后,放出热量为a kJ
B. 当反应达到平衡状态时,X与W的物质的量浓度之比一定为1:2
C. 与使用催化剂相比,△H及两次平衡时各物质的物质的量分数不会改变
D. 若增大Y的浓度,平衡正向移,正反应速率增大,逆反应速率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海藻中含有丰富的碘元素(以I形式存在)。实验室中提取碘的流程如下:

(1)实验操作③的名称是________,所用主要仪器名称为________。
(2)提取碘的过程中,可供选择的有机试剂是________(填序号)。
A.酒精(沸点78 ℃) B.四氯化碳(沸点77 ℃)
C.甘油(沸点290 ℃) D.苯(沸点80 ℃)
(3)在操作②中,溶液中生成少量ICl(ICl的性质类似于氯气),为消除此杂质,使碘全部游离出来,应加入适量________(填序号)溶液,反应的离子方程式___________________。
A.KIO3 B.HClO C.KI D.Br2
(4)利用碘的有机溶液得到单质I2的方法是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化
B.碘水中萃取碘时,往分液漏斗中加入碘水和四氯化碳,充分振荡静置后分液
C.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应
D.实验室中的操作类似“海水煮盐”原理的是蒸发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以下说法正确的是( )
A.H2SO4在电流作用下在水中电离出H+ 和SO42
B.NaCl溶液能导电是因为溶液中有自由移动的Na+ 和Cl
C.由单质X变为X2-的反应是氧化反应
D.某元素处于最高价态时只具有还原性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下等质量的SO2和CO2相比较,下列各项正确的是( )
A. 原子个数之比为1:1B. 物质的量之比为1:1
C. 体积之比为11:16D. 分子数之比为1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电解质水溶液中存在电离平衡、水解平衡、溶解平衡,请回答下列问题。
(1)已知部分弱酸的电离常数如下表:
弱酸 | CH3COOH | HCN | H2CO3 |
电离常数(25℃) | Ka = 1.8×10-5 | Ka=4.3×l0-10 | Ka1=5.0×l0-7 Ka2=5.6×l0-11 |
① 0.1 moI/L NaCN溶液和0.1mol/L NaHCO3溶液中,c(CN-)______c(HCO3-)(填“>”、“<”或“=”)。
②常温下,pH相同的三种溶液:A.CH3COONa B.NaCN C.Na2CO3,其物质的量浓度由大到小的顺序是________(填编号)。
③已知25℃时,CH3COOH(aq)+OH-( aq)=CH3COO-(aq) +H2O △H=-akJ/mol,H+(aq) +OH-(aq) =H2O △H=-b kJ/mol,醋酸电离的热化学方程式为________________。
④将少量CO2通入NaCN溶液,反应的离子方程式是____________________________。
⑤室温下,-定浓度的CH3COONa溶液pH=9,用离子方程式表示溶液呈碱性的原因是______________,溶液中c(CH3COO-)/c(CH3COOH) =___________。
(2)室温下,用0.100 mol/L盐酸溶液滴定20.00mL0.l00mol/L 的某氨水溶液,滴定曲线如图所示(横坐标为盐酸的体积)。
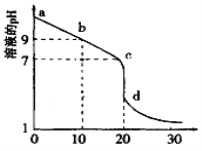
① d点所示的溶液中离子浓度由大到小的顺序依次为____________。
② b点所示的溶液中c(NH3·H2O)-c(NH4+)=_________(用溶液中的其它离子浓度表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温条件下,可逆反应:2NO(g)+O2(g)![]() 2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
2NO2(g)在体积固定的密闭容器中进行,达到平衡状态的标志的是( )
①单位时间内生成n mol O2的同时生成2n mol NO2②单位时间内生成n mol O2的同时生成2n mol NO③用NO2、NO、O2表示的反应速率的比为2:2:1的状态④混合气体的颜色不再改变的状态⑤混合气体的密度不再改变的状态⑥混合气体的压强不再改变的状态⑦混合气体的平均相对分子质量不再改变的状态.
A. ①④⑥⑦ B. ②③⑤⑦ C. ①③④⑤ D. 全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,将一定量的气体通入体积为2L的密闭容器中,使其发生反应,,有关物质X、Y、Z的物质的量的变化如图所示。则下列有关推断正确的是( )

A. 该反应的化学方程式为: 3Z = 3X+2Y
B. t0时,X、Y、Z的质量不再改变
C. t0时,Z的浓度为1.2 mol/L
D. t0时,反应停止,反应速率为0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com