
A、B、C、D是原子序数依次增大的短周期主族元素,A、C在元素周期表中的相对位置如图,A元素最外层与次外层上的电子数之差为3,B为地壳中含最最多的金属元素。
|
A |
|
|
|
C |
(1)D原子结构示意图为_____________。
(2)将C的低价态氧化物甲通入到D单质的水溶液会使之褪色,体现了甲的________性,写出该反应的离子方程式_____________________。
(3)A的最高价氧化物对应的水化物是乙,现将过量Cu加入到100 mL 8.0 mol/L乙的浓溶液中,充分反应,共收集到6.72L(标准状况)气体,则该气体的成分是_______________,还原剂失电子数为_________________。
(4)将两份足量的B单质分别加入到等体积等浓度的盐酸和NaOH溶液中,充分反应生成气体的体积比为____________________,若将反应后所得的溶液混合,会生成白色沉淀,发生反应的离子方程式为___________________________________________________;B单质表面的氧化膜可用NaOH溶液除去,写出该反应的化学方程式____________________________________________________________。
(14分)(1) (1) (2)还原(1分) Cl2+SO2+2H2O=4H++2Cl-+SO42-(2分)
(1) (2)还原(1分) Cl2+SO2+2H2O=4H++2Cl-+SO42-(2分)
(3)NO、NO2(2分) 0.5NA或3.01×1023(2分)
(4)1:3(2分) Al3++3[Al(OH)4]-=4Al(OH)3↓(2分)
Al2O3+2NaOH+3H2O=2Na[Al(OH)4](2分)
【解析】
试题分析:根据A和C元素在周期表中的相对位置可知,A是第二周期元素。A元素最外层与次外层上的电子数之差为3,所以A的原子序数=2+5=7,即A是氮元素,则C是硫元素。B为地壳中含最最多的金属元素,所以B是铝元素。又因为A、B、C、D是原子序数依次增大的短周期主族元素,所以D是氯元素。
(1)氯元素的原子序数是17位于第三周期第 ⅦA族,其原子结构示意图为 。
。
(2)S的低价态氧化物甲是SO2,具有还原性,氯气具有强氧化性,因此SO2能使氯水褪色,二者发生的是氧化还原反应,反应的离子方程式为Cl2+SO2+2H2O=4H++2Cl-+SO42-。
(3)N的最高价氧化物对应的水化物乙是硝酸,属于氧化性酸,其浓溶液与铜反应的方程式为Cu+4HNO3=Cu(NO3)2+2H2O+2NO2↑。100 mL 8.0 mol/L乙的浓溶液中硝酸的物质的量=0.1L×8.0mol/L=0.8mol,如果全部被还原则生成NO2的物质的量是0.4mol,其标准状况下的体积=0.4mol×22.4L/mol=8.96L>6.72L,这说明生成的气体中还含有NO,这是由于随着反应的进行,硝酸的浓度逐渐减小,而稀硝酸的还原产物是NO。混合气的物质的量=6.72L÷22.4L/mol=0.3mol,则根据氮原子守恒可知,生成的硝酸铜的物质的量=(0.8mol-0.3mol)÷2=0.25mol。因此被氧化的铜单质的物质的量=0.25mol,所以还原剂失去电子的个数=0.25×2NA=0.5NA。
(4)铝与盐酸和氢氧化钠溶液反应的化学方程式分别是2Al+6HCl=2AlCl3+3H2↑、2Al+2NaOH+2H2O=2NaAlO2+3H2↑。因此早盐酸和氢氧化钠溶液的体积与浓度都相同的条件下与足量铝反应生成氢气的体积之比是1:3;氯化铝与偏铝酸钠反应生成氢氧化铝白色沉淀,反应的离子方程式为Al3++3[Al(OH)4]-=4Al(OH)3↓。氧化铝是两性氧化物,能溶解在氢氧化钠溶液中,反应的化学方程式为Al2O3+2NaOH+3H2O=2Na[Al(OH)4]。
考点:考查元素、物质推断;SO2和氯气的性质;铜与硝酸反应的计算;铝及其化合物的性质和转化


 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案科目:高中化学 来源: 题型:
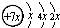 ,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解


| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素C形成的单质可以在点燃条件分别与元素A、B、D形成的单质化合,所得化合物均存在共价键 | B、元素B、C、D的原子半径由大到小的顺序为:r(D)>r(C)>r(B) | C、1.0 L 0.1 mol/L戊溶液中含阴离子总的物质的量小于0.1 mol | D、1 mol甲与足量的乙完全反应共转移约1.204×1024个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com