
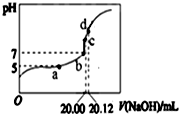
 常温下,用20mL0.1000mol/L NaOH溶液滴定20mL 0.1000mol/L CH3COOH溶液所得滴定曲线如图.下列说法不正确的是( )
常温下,用20mL0.1000mol/L NaOH溶液滴定20mL 0.1000mol/L CH3COOH溶液所得滴定曲线如图.下列说法不正确的是( )| A. | 滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) | |
| B. | a点所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) | |
| C. | d点所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| D. | b和c点所示溶液中:c(OH-)-c(H+)=c(Na+)-c(CH3COO-) |
分析 A.在滴定中当加入碱比较少时,可能出现c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)的情况;
B.a点溶液中溶质为CH3COOH和CH3COONa;
C.d点溶液显碱性,则c(OH-)>c(H+),CH3COO-发生水解浓度减小;
D.根据溶液中电荷守恒分析.
解答 解:A.滴定刚开始时,溶液中滴加的NaOH很少,溶液中存在大量的CH3COOH,溶液中CH3COOH小部分电离,则c(CH3COOH)>c(CH3COO-),所以溶液中可能出现c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-)的情况,故A正确;
B.a点溶液的pH=5,溶液中溶质为CH3COOH和CH3COONa,则c(Na+)<c(CH3COOH)+c(CH3COO-),故B错误;
C.d点溶液显碱性,则c(OH-)>c(H+),CH3COO-发生水解浓度减小,所以c(Na+)>c(CH3COO-),则d点所示溶液中:c(Na+)>c(CH3COO-)>c(OH-)>c(H+),故C正确;
D.b和c点所示溶液中均存在电荷守恒,即正电荷的总浓度等于负电荷的总浓度,即:c(OH-)+c(CH3COO-)=c(H+)+c(Na+),所以c(OH-)-c(H+)=c(Na+)-c(CH3COO-),故D正确.
故选B.
点评 本题考查离子浓度大小比较,题目难度中等,明确混合后溶液中的溶质是解答的关键,注意电荷守恒和物料守恒的应用,试题培养了学生灵活应用能力.


 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案科目:高中化学 来源: 题型:解答题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
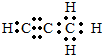 .Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑.
.Q与水反应的化学方程式为Mg2C3+4H2O=2Mg(OH)2+C3H4↑.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
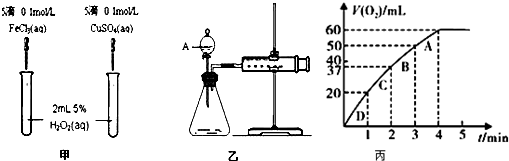
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
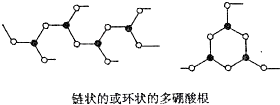
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
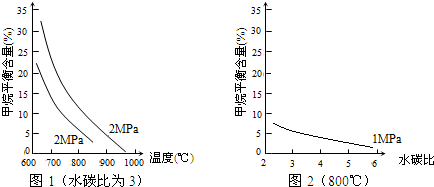
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
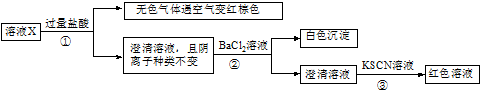
| A. | 无色气体可能是NO和CO2的混合物 | |
| B. | 原溶液可能存在Fe3+ | |
| C. | 溶液X中所含离子种类共有4种 | |
| D. | 另取l00mL原溶液X,加入足量的NaOH溶液,充分反应后过滤,洗涤,灼烧至恒重,理论上得到的固体质量为2.4g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 四种元素均可与氢元素形成 18电子分子 | |
| B. | X、Y、Z、W形成的单质最多有 6种 | |
| C. | 四种元素中,Z的最高价氧化物对应水化物酸性最强 | |
| D. | 四种元素的原子半径:rZ>rX>rY>rW |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
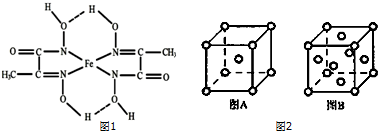
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等物质的量浓度的下列溶液:①H2CO3、②Na2CO3、③NaHCO3、④(NH4)2CO3:其中c(CO32-)的大小关系为:②>④>③>① | |
| B. | pH=2的H2C2O4溶液与pH=12的NaOH溶液等体积混合:c(Na+)+c(H+)=c(OH-)+c(HC2O4-)+c(C2O42-) | |
| C. | 向0.2 mol•L-1NaHCO3 溶液中加入等体积0.1 mol•L-1NaOH 溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,同浓度的CH3COONa与CH3COOH 溶液等体积混合,溶液的pH<7:c(CH3COOH)+c(OH-)>c(Na+)+c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com