
下列有关电解质的电离和水解说法正确的是( )
A.在25℃时,任何水溶液中Kw=1×10-14。
B.在NaHSO4溶液中,c(H+)=c(OH-)+c(SO42-)
C.在pH=2的盐酸酸化的FeCl3溶液,稀释至10倍,则溶液pH=3
D.0.1mol/L醋酸溶液中加入冰醋酸,平衡正向移动,醋酸的电离程度增大
B
【解析】
试题分析:A.在25℃时,在任何物质的稀的水溶液中存在着Kw=1×10-14。如果浓度较大,就不符合。错误。B.在溶液中H+由H2O和NaHSO4
共同电离产生。NaHSO4=Na++H++
SO42-.;H2O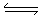 H++OH-.故c(H+)=c(OH-)+c(SO42-)。正确。C.在pH=2的盐酸酸化的FeCl3溶液,若稀释至10倍,若盐水解的程度不变则溶液pH=3,但稀释使FeCl3的水解程度增大故溶液2<pH<3.错误。D.0.1mol/L醋酸溶液中加入冰醋酸,平衡正向移动,但是增加的醋酸比平衡移动减少的醋酸要多,该醋酸的电离程度反而减小。错误。
H++OH-.故c(H+)=c(OH-)+c(SO42-)。正确。C.在pH=2的盐酸酸化的FeCl3溶液,若稀释至10倍,若盐水解的程度不变则溶液pH=3,但稀释使FeCl3的水解程度增大故溶液2<pH<3.错误。D.0.1mol/L醋酸溶液中加入冰醋酸,平衡正向移动,但是增加的醋酸比平衡移动减少的醋酸要多,该醋酸的电离程度反而减小。错误。
考点:考查电解质的电离和水解的知识。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:高中化学 来源: 题型:
| A、强电解质一定是离子化合物 | B、强电解质的饱和溶液一定是浓溶液 | C、强电解质、弱电解质的电离都是吸热过程 | D、弱电解质的电离能力越强,其电离平衡常数越小 |
查看答案和解析>>
科目:高中化学 来源:2015届安徽省宿州市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列有关电解质的说法中正确的是
A.强电解质一定是离子化合物
B.强电解质、弱电解质的电离都是吸热过程
C.强电解质的饱和溶液一定是浓溶液
D.强电解质在水中一定能全部溶解
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com