

| 物质 | 酸 | 碱 | 盐 | 氧化物 |
| 化学式 | ①HCl ②H2SO4(或HNO3、H2CO3) | ③NaOH(或KOH) ④Ba(OH)2 | ⑤Na2CO3 ⑥Na2SO4 | ⑦CO2 ⑧Na2O2 |
分析 (1)以Na、K、H、O、C、S中任意两种或三种元素组成合适的物质任,可组成酸、碱、盐、氧化物等,根据常见的物质书写,酸是水溶液中电离出的阳离子全部是氢离子的化合物,碱是水溶液中电离出的阴离子全部是氢氧根离子的化合物;
(2)根据二氧化碳可以与氢氧化钠反应生成碳酸钠;
(3)过氧化钠中钠元素化合价为+1价,依据元素化合价代数和为0计算得到氧元素化合价,呼吸面具中用⑧作为O2来源的反应是过氧化钠和二氧化碳反应生成碳酸钠和氧气;
(4)根据CO2的检验方法,能使澄清石灰水变浑浊设计检验方法;
(5)计算二氧化碳物质的量n=$\frac{V}{22.4}$,书写化学方程式,依据化学方程式中定量关系计算需要氯化氢的物质的量,结合c=$\frac{n}{V}$计算体积.
解答 解:(1)以Na、K、H、O、C、S中任意两种或三种元素组成合适的物质任,可组成酸有:H2SO4或H2S、H2CO3,碱有:NaOH、KOH,
盐有:Na2CO3、Na2SO4、K2CO3、K2SO4 ,氧化物有:H2O、SO2、SO3、CO、CO2,
故答案为:H2SO4(或HNO3、H2CO3 ),NaOH(或KOH);
(2)⑦转化为⑤的反应为二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,反应的化学方程式:2NaOH+CO2=Na2CO3+H2O,
故答案为:2NaOH+CO2=Na2CO3+H2O;
(3)⑧中氧元素的化合价是-1价,呼吸面具中用⑧作为O2来源的反应原理为过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(4)实验室检验二氧化碳气体,把气体通入澄 清的石灰水,石灰水变浑浊,说明气体为二氧化碳.
故答案为:将气体通入澄清的石灰水中,变浑浊,则说明该气体是CO2;
(5)二氧化碳物质的量n=$\frac{V}{22.4}$=$\frac{11.2L}{22.4L/mol}$=0.5mol,实验室制备CO2用稀盐酸和大理石或石灰石反应,其反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑;需呀的HCl物质的量为0.5mol×2=1mol,需要4mol•L-1的盐酸体积V=$\frac{1mol}{4mol/L}$=0.25L=250ml,故答案为:250.
点评 本题考查物质的分类,题目难度不大,注意H、O、S、N、Na五种元素常见的物质的存在形式,以及物质的分类方法.


 优等生题库系列答案
优等生题库系列答案 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:选择题
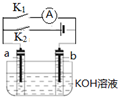
| A. | 断开K2,闭合K1一段时间,溶液的pH要变大 | |
| B. | 断开K1,闭合K2时,b极上的电极反应式为 2H++2e-═H2↑ | |
| C. | 断开K1,闭合K2时,OH-向b极移动 | |
| D. | 断开K2,闭合K1时,a极上的电极反应式为:4OH--4e-═O2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向盛水的烧杯中投入小拇指头大小的钠块,观察现象 | |
| B. | 将一小块钠放在石棉网上加热,观察现象 | |
| C. | 实验后剩余的钠不能放回原瓶 | |
| D. | 用手掰开一块金属钠,观察钠的颜色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Ca(OH)═Ca2++2OH- | B. | KNO3═K++NO3- | C. | NH4Cl═4NH++Cl- | D. | H2SO4═2H++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶质的质量分数w=$\frac{1000a}{17V}$100% | |
| B. | 溶质的物质的量浓度c=$\frac{1000a}{17V}$ (mol/L) | |
| C. | 溶液中c(OH-)=$\frac{b}{V}$ (mol/L) | |
| D. | 上述溶液中再加入VmL水后,所得溶液的质量分数大于0.5w |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe2+.Na+.NO3-.H+ | B. | NH4+.Fe3+.SO42-.SCN- | ||
| C. | SO42-.Cl-.Cu2+.Mg2+ | D. | Ba2+.K+.SO32-.H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 A、B是两种有刺激性气味的气体,其水溶液都有漂白性,且当两者等物质的量通入到有色物质的溶液中时失去漂白性.试根据下列实验事实填空
A、B是两种有刺激性气味的气体,其水溶液都有漂白性,且当两者等物质的量通入到有色物质的溶液中时失去漂白性.试根据下列实验事实填空查看答案和解析>>
科目:高中化学 来源: 题型:解答题
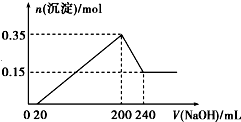
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com