
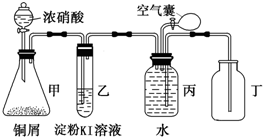
 某校化学兴趣小组用所示装置图验证NO2的氧化性和NO的还原性.请回答下列问题:
某校化学兴趣小组用所示装置图验证NO2的氧化性和NO的还原性.请回答下列问题:

科目:高中化学 来源: 题型:
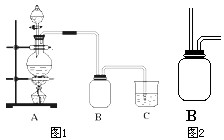 某校化学兴趣小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如图1所示:
某校化学兴趣小组用浓盐酸与二氧化锰加热反应来制取并收集氯气,装置如图1所示:查看答案和解析>>
科目:高中化学 来源: 题型:
已知亚甲基蓝其氧化型呈蓝色,还原型呈无色,其转化关系式为:氧化型(蓝色)+ne-![]() 还原型(无色),奇妙的“蓝瓶子”实验就是利用上述原理,其装置如图1。
还原型(无色),奇妙的“蓝瓶子”实验就是利用上述原理,其装置如图1。
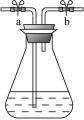
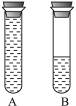
图1 图2
某校化学兴趣小组用图1装置进行下述实验:
①在250 mL锥形瓶中,依次加入2 g NaOH、100 mL H2O和2 g葡萄糖,搅拌溶解后,再加入3~5滴0.2%的亚甲基蓝溶液,振荡混合液呈蓝色;
②塞紧橡皮塞,关闭活塞a、b,静置,溶液变为无色;
③打开活塞、振荡,溶液又变为蓝色;
④关闭活塞、静置,溶液又变为无色;
⑤以上步骤③④可重复多次。
请回答下列问题:
(1)若塞紧图1中锥形瓶塞,并打开导管活塞a、b,从____________导管口(填“左”或“右”)通入足量氦气后,再关闭活塞a、b并振荡,溶液_________(填“能”或“不能”)由无色变为蓝色。
(2)如图2所示:某学生将起初配得的蓝色溶液分装在A、B两支试管中,A试管充满溶液,B中有少量溶液,塞上橡皮塞静置片刻,两溶液均显无色。若再同时振荡A、B试管,溶液显蓝色的是_________试管。
(3)上述转化过程中葡萄糖的作用是_________,亚甲基蓝的作用是_________。
(4)上述实验中葡萄糖也可用鲜橙汁(其中含丰富维生素C)代替,这是因为____________________________________。
(5)该实验中③④操作_________(填“能”或“不能”)无限次重复进行,理由是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学兴趣小组用如图所示过程除去AlCl3中含有的Mg2+、K+杂质离子,并尽可能减少AlCl3的损失。请回答下列问题:
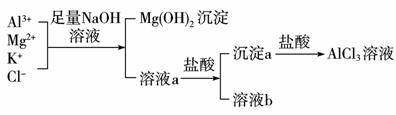
(1)写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应
的离子方程式:____________、____________、____________。氢氧化钠溶液能否用氨水代替,为什么?____________
____________ 。
(2)溶液a中存在的离子有____________;在溶液a中加入盐酸
时需控制溶液的pH,为什么?____________;为此,改进方法是____________。
查看答案和解析>>
科目:高中化学 来源:2012届山东省曲阜师大附中高三9月教学质量检测化学试卷 题型:填空题
( 12 分)(1)某校化学兴趣小组用如下图所示过程除去AlCl3中含有的Mg2+、K+杂质离子并尽可能减少AlCl3的损失。请回答下列问题:
①写出混合物中加入足量氢氧化钠溶液时,溶液中发生反应的离子方程式:
。
②溶液a中存在的阴离子有__________________;在溶液a中加入盐酸时需控制溶液的pH的原因是_______________________________________;为此,改进方法是 。
?(2)?该化学小组又测定一定质量的某镁铝混合物中镁的质量分数,设计了如下实验方案:
方案Ⅰ:镁铝混合物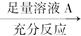 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:镁铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是 ?(填代号)
| A.溶液A选用NaOH溶液 |
| B.若溶液B选用浓硝酸,则测得镁的质量分数偏小 |
| C.溶液A和B均可选用稀硝酸 |
| D.实验室中方案Ⅱ更便于实施 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com