
分析 硫酸氢钠为强电解质,水中完全电离;NaHSO4与Ba(OH)2在溶液中按物质的量2:1混合,反应生成硫酸钡、硫酸钠和水.
解答 解:硫酸氢钠为强电解质,水中完全电离,电离方程式:NaHSO4=Na++H++SO42-;
NaHSO4与Ba(OH)2在溶液中按物质的量2:1混合,反应生成硫酸钡、硫酸钠和水,离子方程式:Ba2++2OH-+2H++SO42-=2H2O+BaSO4↓;
故答案为:NaHSO4=Na++H++SO42-;Ba2++2OH-+2H++SO42-=2H2O+BaSO4↓.
点评 本题考查了电解质电离方程式的书写、离子方程式的书写,明确电解质强弱是解题关键,注意反应物用量对离子反应的影响,题目难度不大.


 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL0.1mol•L-1FeCl3溶液中含有Fe3+的数目为0.01NA | |
| B. | 在铜与单质硫的反应中,1mol铜失去的电子数为2NA | |
| C. | 15.6g由Na2S和Na2O2组成的固体混合物中,含有的阴离子数为0.2NA | |
| D. | 104g苯乙烯(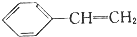 )中含有碳氢键的数目和碳碳双键的数目分别为8NA和4NA )中含有碳氢键的数目和碳碳双键的数目分别为8NA和4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应后溶液中铁元素可能以Fe2+形式存在 | |
| B. | 反应后溶液中c(N03-)=0.85 mol/L | |
| C. | 反应后的溶液最多还能溶解1.4 g Fe | |
| D. | 1.12 L气体可能是NO、NO2的混合气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 粒子 | 操作 | 现象 | 现象 | |
| a | H+ | |||
| b | Cl- | |||
| c | Cl2 | |||
| d | HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①③ | B. | 只有②③ | C. | ①②③④ | D. | 只有③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 整个过程中,H20的电离度逐渐增大 | B. | c(Na+)>c(HS-)>c(H+)>c(S2-)>c(0H-) | ||
| C. | c(Na+)+c(H+)═c(0H-)+c(HS-)+2c(S2-) | D. | c(Na+)═c(HS-)+c(H2S) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com