
| A.铅蓄电池在放电过程中,负极质量减小,正极质量增加 |
| B.常温下,反应C(s)+CO2(g)=2CO(g)不能自发进行,则该反应的ΔH>0 |
| C.钢铁在潮湿的空气中会形成原电池而被腐蚀,其正极反应为:O2 + 2H2O + 4e-=4OH- |
| D.原子结合成分子的过程一定释放出能量 |
科目:高中化学 来源:不详 题型:单选题
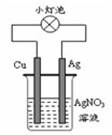
| A.该装置实现电能转变为化学能 |
| B.正极是Cu、负极是Ag |
| C.电子由Ag棒转移到Cu棒 |
| D.Ag棒上的电极反应为:Ag++e-=Ag |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
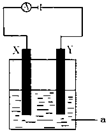
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
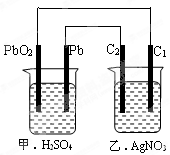 ⑵乙装置中C1电极为
⑵乙装置中C1电极为 | A.正极 | B.负极 | C.阴极 | D.阳极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
 ⑶ 取步骤⑵中的滤渣,将其分为两等份,每一份质量为8.0g。将其中一份在氧气流中充分灼烧,生成的气体全部通入足量的澄清石灰水,得到干燥、纯净的沉淀20.0 g。据此计算8.0 g滤渣中活性炭的质量为 ;
⑶ 取步骤⑵中的滤渣,将其分为两等份,每一份质量为8.0g。将其中一份在氧气流中充分灼烧,生成的气体全部通入足量的澄清石灰水,得到干燥、纯净的沉淀20.0 g。据此计算8.0 g滤渣中活性炭的质量为 ; ,冷却、称量,得到6.86g固体。
,冷却、称量,得到6.86g固体。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
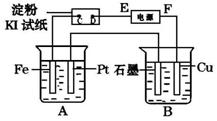
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
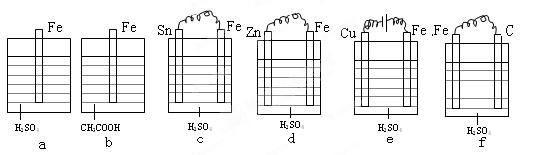
| A.e>d>a>b>c>f | B.e>f>c>a>b>d | C.e>c>f>a>b>d | D.e>f>d>a>b>c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com