
工业上用重晶石(BaSO4)制备BaCO3的常用方法主要有高温锻烧还原法、沉淀转化法等。高温煅烧还原法的工艺流程可简单的表示如下:
(1)若“煅烧”时产生一种有毒的还原性气体,则反应的化学方程式为______。
(2)工业上煅烧重晶石矿粉时,为使BaSO4得到充分的还原和维持及应所需的高温,应采取的措施是______。
a.加人过量的炭,同时通入空气 b.设法将生成的BaS及时移出
(3)在第一次过滤后洗涤,检验是否洗涤干净的试剂最好是______。
(4)沉淀转化法制备BaCO3可用饱和Na2CO3溶液将BaSO4转化为BaCO3:
BaSO4 (s)+CO32-(aq) BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)
则:①在实验室将少量BaSO4固体全部转化为BaCO3的实验操作方法与步骤为______。
②与高温煅烧还原法相比,沉淀转化法的优点主要有______。
③已知:Ksp(BaCO3)=2.40×10-9,Ksp(BaSO4)=1.20×10-10。现欲用沉淀转化法将BaSO4转化为BaCO3,该反应的平衡常数为______。如用1.00 L 0. 210 mol ? L-1 Na2CO3溶液处理,试计算BaSO4被转化的质量______(要有计算过程,结果保留3位有效数字)。
(18分)
(1)BaSO4+4C BaS+4CO↑(3分)
BaS+4CO↑(3分)
(2)a(2分)
(3)H2SO4(2分,其它合理答案也给分)
(4)①将适量饱和Na2CO3溶液加入BaSO4固体中,充分搅拌,静置、弃去上层清液;如此操作,反复多次(直到BaSO4全部转化为BaCO3)(3分)
②节能、环保等(2分)
③5×10-2(2分)
解:设BaSO4被转化的物质的量为xmol,则碳酸根离子的变化浓度为xmol/L,即:
BaSO4 (s)+CO32-(aq) BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)
起始浓度/mol?L-1 0.210 0
变化浓度/mol?L-1 x x
起始浓度/mol?L-1 0.210—x x (1分)
由于K= =
= ,则
,则 =
= (1分)
(1分)
解得:x=0.0100(1分)
由于m=n?M,则BaSO4被转化的质量为0.0100mol×233g/mol=2.33g(1分)
答:BaSO4被转化的质量为2.33g。
解析试题分析:(1)依题意,BaSO4与C在高温下发生氧化还原反应,生成BaS和CO,硫元素由+6降为—2价,碳元素由0升为+2价,根据化合价升降总数相等、原子个数守恒,则该反应为BaSO4+4C BaS+4CO↑;(2)加入过量的碳,同时通入空气,可以使C与氧气反应,该反应是放热反应,碳过量不仅能使硫酸钡充分还原,还能维持反应所需的高温,故a正确;硫化钡是固体,固体物质的浓度是常数,将生成的硫化钡及时移走,不能使平衡向正反应方向移动,故b错误;(3)硫化钡是强碱弱酸盐,能溶于水,且与水反应生成氢氧化钡和硫化氢气体,氢氧化钡是可溶性强碱,过量的碳或未完全反应的硫酸钡等难溶于水,过滤所得滤渣的主要成分是碳或硫酸钡等物质,滤渣能吸附可溶性的钡离子、氢氧根离子,钡离子遇硫酸产生白色的硫酸钡沉淀,因此取最后一次洗涤液少许于试管,滴入少量稀硫酸,若产生白色沉淀,说明沉淀未洗涤干净;反之,则洗涤干净;另外,选择酚酞等指示剂也可以检验是否含有氢氧根离子;(4)根据浓度对平衡移动的影响规律,增大碳酸根离子浓度,可以使沉淀平衡右移,则设计的实验方案为①将适量饱和Na2CO3溶液加入BaSO4固体中,充分搅拌,静置、弃去上层清液;如此操作,反复多次(直到BaSO4全部转化为BaCO3);②高温煅烧法需要消耗能量,产生有毒的硫化氢气体,步骤多,而沉淀转化法则节约能源,环保,操作步骤少等;③设BaSO4被转化的物质的量为xmol,则碳酸根离子的变化浓度为xmol/L,即:
BaS+4CO↑;(2)加入过量的碳,同时通入空气,可以使C与氧气反应,该反应是放热反应,碳过量不仅能使硫酸钡充分还原,还能维持反应所需的高温,故a正确;硫化钡是固体,固体物质的浓度是常数,将生成的硫化钡及时移走,不能使平衡向正反应方向移动,故b错误;(3)硫化钡是强碱弱酸盐,能溶于水,且与水反应生成氢氧化钡和硫化氢气体,氢氧化钡是可溶性强碱,过量的碳或未完全反应的硫酸钡等难溶于水,过滤所得滤渣的主要成分是碳或硫酸钡等物质,滤渣能吸附可溶性的钡离子、氢氧根离子,钡离子遇硫酸产生白色的硫酸钡沉淀,因此取最后一次洗涤液少许于试管,滴入少量稀硫酸,若产生白色沉淀,说明沉淀未洗涤干净;反之,则洗涤干净;另外,选择酚酞等指示剂也可以检验是否含有氢氧根离子;(4)根据浓度对平衡移动的影响规律,增大碳酸根离子浓度,可以使沉淀平衡右移,则设计的实验方案为①将适量饱和Na2CO3溶液加入BaSO4固体中,充分搅拌,静置、弃去上层清液;如此操作,反复多次(直到BaSO4全部转化为BaCO3);②高温煅烧法需要消耗能量,产生有毒的硫化氢气体,步骤多,而沉淀转化法则节约能源,环保,操作步骤少等;③设BaSO4被转化的物质的量为xmol,则碳酸根离子的变化浓度为xmol/L,即:
BaSO4 (s)+CO32-(aq) BaCO3(s)+SO42-(aq)
BaCO3(s)+SO42-(aq)
起始浓度/mol?L-1 0.210 0
变化浓度/mol?L-1 x x
起始浓度/mol?L-1 0.210—x x (1分)
由于K= =
= =
= =5×10-2
=5×10-2
则 =
= =5×10-2(1分)
=5×10-2(1分)
解得:x=0.0100(1分)
由于m=n?M,则BaSO4被转化的质量为0.0100mol×233g/mol=2.33g(1分)。
考点:考查有关物质制备的化学工艺流程,涉及关键环节化学方程式的书写、检验沉淀是否洗净、设计实验方案、根据溶度积求平衡常数和沉淀被转化的质量等。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
丙酸的结构为CH3—CH2—COOH,丙酸盐是安全有效的防霉、防腐剂,一种以碱式碳酸锌为原料的生产工艺流程如下: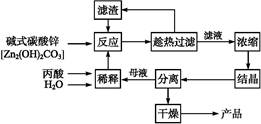
| 序号 | n(丙酸)∶ n(碱式碳酸锌) | 反应温度/℃ | 丙酸锌产率/% |
| 1 | 1∶0.25 | 60 | 67.2 |
| 2 | 1∶0.25 | 80 | 83.5 |
| 3 | 1∶0.25 | 100 | 81.4 |
| 4 | 1∶0.31 | 60 | 89.2 |
| 5 | 1∶0.31 | 80 | 90.1 |
| 6 | 1∶0.31 | 100 | 88.8 |
 ,反应温度 ℃。
,反应温度 ℃。 查看答案和解析>>
科目:高中化学 来源: 题型:填空题
分子筛具有均匀的微孔结构,分子筛筛分作用见下图。由于分子筛具有吸附能力高,热稳定性强等其它吸附剂所没有的优点,使得分子筛获得广泛的应用。某种型号的分子筛的工业生产流程可简单表示如下:

在加NH3·H2O调节pH的过程中,若pH控制不当会有Al(OH)3生成,假设生产流程中铝元素和硅元素均没有损耗,钠原子的利用率为10%。
(1)分子筛的孔道直径为4A(1 A=10-10m)称为4A型分子筛,当Na+被Ca2+取代时就制得5A型分子筛,当Na+被K+取代时就制得3A型分子筛。要高效分离正丁烷(分子直径为4.65A)和异丁烷(分子直径为5.6A)应该选用 型分子筛。
(2)A12(SO4)3溶液与Na2SiO3溶液反应生成胶体的离子方程式为
(3)该生产流程中所得滤液里含有的离子除H+、OH-外,主要为 ;检验其中金属阳离子的操作方法是
(4)加NH3·H2O调节pH后,加热到90℃并趁热过滤的原因可能是
(5)该生产流程中所得分子筛的化学式为
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
磷酸亚铁锂LiFePO4是一种新型汽车锂离子电池的电极材料。某化工厂以铁红、锂辉石LiAl(SiO3)2(含少量Ca2+、Mg2+的盐)、碳粉等原料来生产磷酸亚铁锂。其主要工艺流程如下: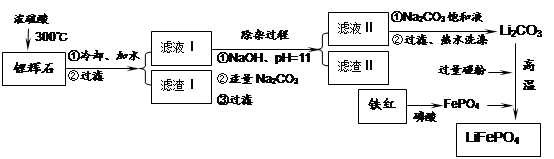
已知:2LiAl(SiO3)2 + H2SO4(浓) 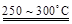 Li2SO4 + Al2O3·4SiO2·H2O↓
Li2SO4 + Al2O3·4SiO2·H2O↓
| 温度/℃ | 20 | 40 | 60 | 80 |
| 溶解度(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| 溶解度(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
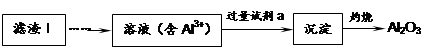
 LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应: 。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为 。
LiFePO4,电池中的固体电解质可传导Li+。试写出该电池放电时的正极反应: 。若用该电池电解饱和食盐水(电解池电极均为惰性电极),当电解池两极共有4480mL气体(标准状况)产生时,该电池消耗锂的质量为 。查看答案和解析>>
科目:高中化学 来源: 题型:填空题
以地下卤水(主要含NaCl,还有少量Ca2+、Mg2+)为主要原料生产亚硫酸钠的新工艺如下,同时能得到用作化肥的副产品氯化铵。
已知以下四种物质的溶解度曲线图:
(1)“除杂”时,先加入适量石灰乳过滤除去Mg2+,再通入CO2并用少量氨水调节pH过滤除去Ca2+,“废渣”的主要成分为 、 。
(2)“滤渣1”的化学式为 。
(3)在“滤液1”中加入盐酸的目的是 。“滤渣2”的化学式为 。
(4)已知H2CO3和H2SO3的电离常数如下表,“通入SO2”反应的化学方程式为 。
| 物质 | 电离常数(25℃) |
| H2CO3 | K1=4.4X10-7 K2=4.7X10-11 |
| H2SO3 | K1=1.23X10-2 K2=5.6X10-8 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在硫酸工业生产中,为了有利于SO2的转化,且能充分利用热能,采用了中间有热交换器接触室(见图)。按此密闭体系中气体的流向,则在A处流出的气体为( )
| A.SO2 | B.SO3、O2 | C.SO2、SO3 | D.SO2、O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
化学工业是国民经济的支柱产业,下列生产过程中不涉及化学变化的是
| A.化工厂用氯气制漂白粉 | B.冶炼厂用氧化铝生产铝 |
| C.硝酸厂用氨制硝酸 | D.炼油厂分馏法生产汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列物质的制备,符合工业生产实际的是( )
| A.将氯气通入澄清石灰水中制漂白粉 |
| B.用离子交换膜法电解饱和食盐水制备烧碱、氢气和氯气 |
| C.将氢气和氯气混合后点燃,产物用水吸收制备盐酸 |
| D.将SO2和O2的混合气加高压后,通过接触室,制备SO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
(1)1791年,法国医生路布兰首先获得制碱专利,以食盐、浓硫酸、石灰石、煤为原料制碱,该方法分三步:
①用NaCl与H2SO4反应制Na2SO4;2NaCl+H2SO4 Na2SO4+2HCl↑
Na2SO4+2HCl↑
②用焦炭还原Na2SO4制Na2S;Na2SO4+4C Na2S+4CO↑
Na2S+4CO↑
③用硫化钠与石灰石反应制Na2CO3;Na2S+CaCO3 Na2CO3+CaS
Na2CO3+CaS
(2)下列说法正确的是 ( )。
| A.②③两步都是氧化还原反应 |
| B.只有第②步是氧化还原反应 |
| C.该方法对生产设备基本没有腐蚀 |
| D.该方法对环境污染较小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com