
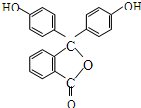
| A. | 酚酞的分子式是C20H12O4 | B. | 分子中的所有碳原子不在同一平面 | ||
| C. | 1mol酚酞最多可能消耗2mol NaOH | D. | 1mol酚酞可与10mol H2加成 |
分析 由结构简式可知,含C、H、O三种元素,分子中含16个H,含酚-OH和-COOC-,结合酚及酯的性质来解答.
解答 解:A.由结构简式可知酚酞的分子式是C20H14O4,故A错误;
B.每个苯环中的碳原子在一个平面上,但是据有甲烷结构的碳原子可定和它们不共面,故B正确;
C.酯基能水解后生成的羧基、酚羟基有酸性,他们均和氢氧化钠反应,1mol酚酞最多可消耗3molNaOH,故C错误;
D.能与氢气发生加成的反应的为苯环,则1mol酚酞可与9mol H2加成,故D错误.
故选B.
点评 本题考查有机物的结构与性质,为高频考点,把握有机物的官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意物质组成和类别的判断,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用重结晶法可除去KNO3晶体中混有少量NaCl晶体 | |
| B. | 实验室制取乙酸丁酯时用水浴加热 | |
| C. | 在硫酸钡悬浊液中加入足量饱和碳酸钠溶液可将其转化为碳酸钡 | |
| D. | 二氧化硫分别通入到硫化钠和硝酸钡溶液中产生沉淀可证明二氧化硫的氧化性和还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
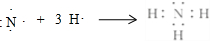
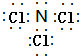
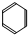 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
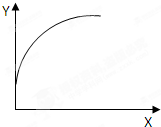 在一密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)=2C(g)+Q(Q>0),当达到平衡后,改变一个条件(X),下列量(Y)一定符合图中曲线的是( )
在一密闭容器中通入A、B两种气体,在一定条件下反应:2A(g)+B(g)=2C(g)+Q(Q>0),当达到平衡后,改变一个条件(X),下列量(Y)一定符合图中曲线的是( )| X | Y | |
| A | 温度 | 混合气体平均相对分子质量 |
| B | 再加入C | A的质量分数 |
| C | 再加入A | B的转化率 |
| D | 压强 | B的浓度 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-COOH | B. | CH2=CH-COOCH3 | C. | CH3CH2OH | D. | CH2=CH-CH2OH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
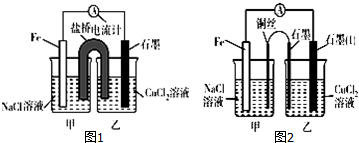
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com