
分析 (1)次外层有2个电子,则有2个电子层,最外层有3个未成对电子,其电子排布式为:1s22s22p3;
(2)在原子中,核电荷数=核内质子数=核外电子数,B元素原子的核电荷数为n,X得到1个电子后变为B-,C失去1个电子后变为C+,根据电子层结构相同,即核外电子数相同,列出等式求解即可;
(3)M能层上有3个能级,分别为3s、3p、3d能级,其中s能级最多有2个电子,p能级最多有6个电子,d能级最多有10个电子;
(4)D元素的正三价离子的3d轨道为半充满,3d轨道电子数为5,应为Fe元素;
(5)某元素的基态原子最外层电子排布为3s23p2,应为Si元素,核外电子排布为1s22s22p63s23p2.
解答 解:(1)基态原子的最外层有3个未成对电子,次外层有2个电子的元素,其电子排布式为:1s22s22p3,符号为N,故答案为:N;
(2)设元素B的核电荷数是a,C元素原子的核电荷数为b,因为阴离子B-与阳离子C+电子层结构都与氩相同相同,即核外电子数相同,所以a=18-1=17,b=18+1=19,所以B是Cl,C为K原子,故答案为:Cl;K;
(3)M能层上有3个能级,分别为3s、3p、3d能级,共有9个轨道,其中s能级最多有2个电子,p能级最多有6个电子,d能级最多有10个电子,作为内层最多可容纳18个电子,
故答案为:3;9;18;
(4)D元素的正三价离子的3d轨道为半充满,3d轨道电子数为5,则基态原子的电子排布式为1s22s22p63s23p63d64s2,应为Fe元素,
故答案为:Fe;1s22s22p63s23p63d64s2;
(5)某元素的基态原子最外层电子排布为3s23p2,应为Si元素,核外电子排布为1s22s22p63s23p2,它的次外层能级为2s22p6,有s、p两种不同轨道,电子云形状有2种,原子中所有电子占有8个轨道,其中1s、2s共2个轨道,3个2p轨道,2个3p轨道,原子核外共有14个电子,则有14种不同的运动状态,
故答案为:2;8;14.
点评 本题综合考查原子核外电子排布以及原子结构与元素周期表知识,侧重于基础知识的考查,为高考高频考点,注意相关基础知识的积累,难度不大.


科目:高中化学 来源: 题型:选择题
| c(H2)/mol•L-1 | c(Cl2)/mol•L-1 | v/(mol•L-1•s-1) |
| 1.0 | 1.0 | 1.0k |
| 2.0 | 1.0 | 2.0k |
| 2.0 | 4.0 | 4.0k |
| A. | m=1,n=1 | B. | m=$\frac{1}{2}$,n=$\frac{1}{2}$ | C. | m=$\frac{1}{2}$,n=1 | D. | m=1,n=$\frac{1}{2}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cr2O72-不能将SO2氧化 | B. | 还原性:Cr3+>Fe2+>SO2 | ||
| C. | 氧化性:Cr2O72->Fe3+>SO2 | D. | 两个反应中Fe3+均表现还原性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).
某物质只含C、H、O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表单键、双键等化学键).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
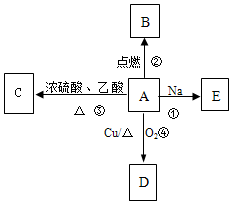 A是易溶于水的有机物C2H5OH,能发生如图所示的多种反应(部分产物已略),D的相对分子质量为44,分子式为C2H4O.请回答下列问题:
A是易溶于水的有机物C2H5OH,能发生如图所示的多种反应(部分产物已略),D的相对分子质量为44,分子式为C2H4O.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/mol•L-1 | 0.64 | 0.50 | 0.50 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com