
| A. | C(Na+)=C(CO32-)+C(HCO3-)+C(OH-) | |
| B. | C(Na+)+C(H+)=C(CO32-)+C(HCO3-)+C(OH-) | |
| C. | C(Na+)+C(H+)=2C(CO32-)+C(HCO3-)+C(OH-) | |
| D. | C(CO32-)+2C(OH-)=3C(H2CO3)+C(HCO3-)+2C(H+) |
分析 n (CO2)=0.2mol,n(NaOH)=0.3mol,
则反应的可能方程式有:CO2+2NaOH=Na2CO3+H2O,CO2+NaOH=NaHCO3,
则有:2>$\frac{n(NaOH)}{n(C{O}_{2})}$=$\frac{3}{2}$>1,
所以:所得产物为Na2CO3和NaHCO3,
设所得产物中含Na2CO3为xmol,NaHCO3为ymol,
则得方程组:$\left\{\begin{array}{l}{x+y=0.2}\\{2x+y=0.3}\end{array}\right.$解得:x=0.1,y=0.1,
在含等物质的量的碳酸钠、碳酸氢钠的溶液中,以此来解答.
解答 解:A、根据电荷守恒可知:C(Na+)+C(H+)=2C(CO32-)+C(HCO3-)+C(OH-),而C(H+)≤C(CO32-),故A错误;
B、根据电荷守恒可知:C(Na+)+C(H+)=2C(CO32-)+C(HCO3-)+C(OH-),故B错误;
C、根据电荷守恒可知:C(Na+)+C(H+)=2C(CO32-)+C(HCO3-)+C(OH-),故C正确;
D、电荷守恒可知:C(Na+)+C(H+)=2C(CO32-)+C(HCO3-)+C(OH-)…①,物料守恒可知:2C(Na+)=3[C(HCO3-)+C(CO32-)+C(H2CO3)…②,将①代入②得:C(CO32-)+2C(OH-)=3C(H2CO3)+C(HCO3-)+2C(H+),故D正确;
故选CD.
点评 本题考查离子浓度大小的比较,确定溶液中的溶质及物质的量的关系是解答本题的关键,然后电荷守恒和物料守恒解答即可,题目难度中等.


 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 硅晶体是一种重要的半导体材料 | |
| B. | 石墨可用做绝缘材料 | |
| C. | 漂白粉的有效成分是次氯酸钙 | |
| D. | 常温下,运输浓硫酸、浓硝酸时可用铝制或铁制槽车 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
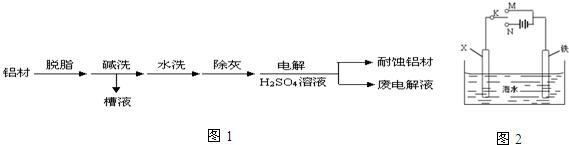
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 测定某浓度盐酸的pH时,先将pH试纸用蒸馏水湿润 | |
| B. | 容量瓶用蒸馏水洗净、必须烘干后才能用于溶液的配制 | |
| C. | 用苯萃取溴水中的溴之后进行分液时,水层从分液漏斗的下口放出 | |
| D. | 中和滴定时,锥形瓶不需要用待测液润洗后就能使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用Fe2+将饮用水中少量ClO2-氧化成为Cl-:4Fe2++ClO2-+4H+═4Fe3++Cl-+2H2O | |
| B. | 向烧碱溶液中加入铝:Al+2OH-═AlO2-+H2↑ | |
| C. | 用过量氨水吸收烟道气中的SO2:SO2+2NH3•H2O═SO32-+2NH4++H2O | |
| D. | 将饱和FeCl3溶液滴入沸水中制取Fe(OH)3胶体:Fe3++3H2O?Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
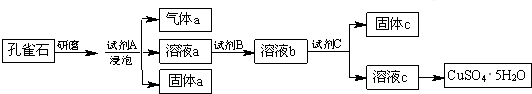
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等.工业上可用H2与重晶石(BaS04)在高温下反应制备BaS,热化学方程式为BaS04(s)+4H2(g)?BaS(s)+4H20(g)△H=+xkJ•mol-1(x>0).回答下列问题:
BaS是一种白色晶体,微溶于水,可用于制备立德粉、Na2S等.工业上可用H2与重晶石(BaS04)在高温下反应制备BaS,热化学方程式为BaS04(s)+4H2(g)?BaS(s)+4H20(g)△H=+xkJ•mol-1(x>0).回答下列问题:| 时间/min | 0 | t | 2t | 3t | 4t |
| n(H2)/mol | 2.00 | 1.50 | n | 0.90 | 0.80 |
| 试验编号 | T/℃ | c起始(H2)/mol•L-1 | 重晶石的比表面积/m2•g-1 |
| Ⅰ | 850 | c1 | 3.4 |
| Ⅱ | T1 | 0.80 | 7.6 |
| Ⅲ | 900 | 0.80 | 7.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素电负性:Ti<Ga | |
| B. | 第二电离能(I2):Na>Mg | |
| C. | 金属晶体的晶胞中空间利用率:体心立方堆积>面心立方堆积. | |
| D. | 晶格能:NaCl>MgO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①-⑤-②-①-④-③ | B. | ①-⑤-⑥-②-④-③ | C. | ③-④-②-⑥-⑤-① | D. | ②-⑤-①-④-③-⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com