
《有机化学基础》
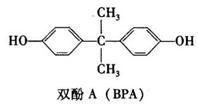 Ⅰ(8分)双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如右下图所示。
Ⅰ(8分)双酚A (也称BPA)常用来生产防碎塑料聚碳酸酯。BPA的结构简式如右下图所示。
(1)双酚A中的含氧官能团为 ▲ (填名称)。
(2)下列关于双酚A的叙述中,不正确的是 ▲ (填标号)。
A.遇FeCl3溶液变色
B.可以发生还原反应
C.1 mol双酚A最多可与2 mol Br2反应
D.可与NaOH溶液反应
(3)双酚A的一种合成路线如下图所示:

①丙烯→A的反应类型是 ▲ 。
②B→C的化学方程式是 ▲ 。
Ⅱ(7分)甲苯和溴乙烷混合物可通过如下流程进行分离。
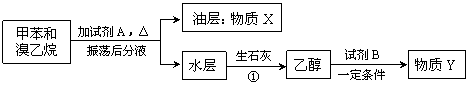 |
请填写下列空白:
(1)X的结构简式为 ▲ ;
(2)操作①能否用分液 ▲ ,理由是 ▲ 。
(3)写出甲苯与溴乙烷的混合物中加入试剂A时发生反应的化学方程式: ▲ 。
(4)如果Y为乙烯,则试剂B为 ▲ ,“一定条件”是指 ▲ 。
科目:高中化学 来源: 题型:
能够证明甲烷构型是四面体的事实是 ( )
A.甲烷的四个键键能相同 B.甲烷的四个键键长相等
C.甲烷的所有C-H键键角相等 D.二氯甲烷没有同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A.铁溶于盐酸中 2Fe + 6H+  = 2Fe3+ + 3H2↑
= 2Fe3+ + 3H2↑
B.碳酸钠与硫酸溶液反应 CO32ˉ + H+ = CO2↑+ H2O
C.二氧化硫被烧碱溶液吸收 SO2 +2OHˉ = SO32ˉ + H2O
D.铜与稀硝酸反应 Cu + 8H+ + 2NO3ˉ= Cu2+ + 2NO↑ + 4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质应用的叙述中,不正确的是
A.氢氧化铝可用于治疗胃酸过多 B.ClO2用于饮用水消毒
C.水玻璃浸泡过的木材既能防腐又能耐火 D.Si用于制造光导纤维
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA表示阿伏加德罗常数的值,下列叙述中正确的是
A.常温下,1 mol Cl2与足量NaOH溶液完全反应,转移的电子数2NA
B.常温常压下,11.2 L CO2中含有的分子数是0.5NA
C.标准状况下,22.4 L水所含原子数为3NA
D.常温常压下,48 g O3和O2的混合气体中氧原子数为3NA
查看答案和解析>>
科目:高中化学 来源: 题型:
设NA为阿伏加德罗常数的数值,下列叙述正确的是(相对原子量:H—1 C—12)
A.1 mol/L氯化铜溶液中的Cu2+数小于NA
B.标准状况下,22.4 L Cl2参加任何化学反应转移的电子数都是2NA
C.28 g聚乙烯含有的碳原子数为2NA
D.1 mol CH5+所含电子数为8NA
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,在体积为3 L的密闭容器中反应:CO(g)+ 2H2(g) CH3OH(g)达到化学平衡状态。
CH3OH(g)达到化学平衡状态。
(1)该反应的平衡常数表达式K= ;
根据右图,升高温度,K值将 (填“增大”、“减小”或“不变”)。
(2)500℃时,从反应开始到达到化学平衡,以H2的浓度变化表示的化学反应速率是 (用nB、tB表示)。
(3)判断该可逆反应达到化学平衡状态的标志是 (填字母)。
a、CO、H2、CH3OH的浓度均不再变化 b、混合气体的密度不再改变
c、混合气体的平均相对分子质量不再改变 d、 v生成(CH3OH)= v消耗(CO)
(4)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是 (填字母)。
a、c(H2)减少 b、正反应速率加快,逆反应速率减慢
c、CH3OH 的物质的量增加 d、重新平衡时c(H2)/ c(CH3OH)减小
(5)根据题目有关信息,请在右下坐标图中标示出该 化学反应过程的能量变化(标明信息)。
 (6)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,该电池中负极上的电极反应式是:2CH3OH–12e-+16OH-= 2CO32-+ 12H2O ,则正极上发生的电极反应为: 。
(6)以甲醇、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池。已知该燃料电池的总反应式为:2CH3OH +3O2+4OH- = 2CO32- + 6H2O,该电池中负极上的电极反应式是:2CH3OH–12e-+16OH-= 2CO32-+ 12H2O ,则正极上发生的电极反应为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是
A.离子化合物中一定含有离子键
B.含有共价键的化合物一定是共价化合物
C.常温常压下,18 g D2O含有6.02×1024个电子
D.标准状况下,11.2L四氯化碳所含3.01×1023个分子
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A、B、C、D之间的转化关系如图所示。下列说法正确的是
 A. 若A为Fe,D为氢气,则B一定为酸
A. 若A为Fe,D为氢气,则B一定为酸
B. 若A、D为化合物,B为水,则C一定是气体单质
C. 若A、B、C、D均为化合物,该反应一定属于复分解反应
D. 若A、B、C、D均为10电子微粒,且C是可使湿润的红色石蕊试纸变蓝的气体,则D常温下一定呈液态
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com