
| A. | 复分解反应一定都不属于氧化还原反应 | |
| B. | 在氧化还原反应中,反应物中的金属单质不一定是还原剂 | |
| C. | 在氧化还原反应中,非金属单质不一定是氧化剂 | |
| D. | 置换反应一定都属于氧化还原反应 |
分析 A.复分解反应中一定没有元素的化合价变化;
B.金属单质在反应中元素的化合价一定升高;
C.非金属单质在反应中元素的化合价可能升高,也可能降低;
D.置换反应中一定存在元素的化合价变化.
解答 解:A.复分解反应中一定没有元素的化合价变化,则复分解反应一定都不属于氧化还原反应,故A正确;
B.金属单质在反应中元素的化合价一定升高,一定为还原剂,故B错误;
C.非金属单质在反应中元素的化合价可能升高,也可能降低,如氢气与氯气反应时H元素的化合价升高,为还原剂,则在氧化还原反应中,非金属单质不一定是氧化剂,故C正确;
D.置换反应中一定存在元素的化合价变化,则置换反应一定都属于氧化还原反应,故D正确;
故选B.
点评 本题考查氧化还原反应与基本反应类型的关系,明确反应中元素的化合价变化是解答本题的关键,题目难度不大.


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
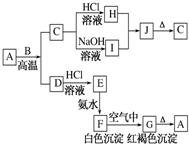 A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.
A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.
草酸亚铁晶体(FeC2O4•2H2O)呈淡黄色.某课题组为探究草酸亚铁晶体的化学性质,进行了一系列实验探究.| 实验步骤(不要求写出具体操作过程) | 预期实验现象和结论 |
| 取少量黑色固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
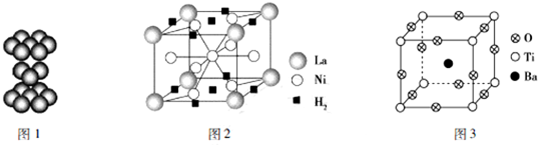
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合金 | B. | 硅酸盐材料 | C. | 有机高分子材料 | D. | 无机非金属材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| H2(g) | Cl2 (g) | HCl (g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | 436 | 243 | a |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
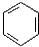 +CH3CO+HBr$\stackrel{ZnCI_{2}}{→}$
+CH3CO+HBr$\stackrel{ZnCI_{2}}{→}$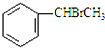 +H2O(卤烷基化反应)
+H2O(卤烷基化反应) +R′-X$\stackrel{一定条件}{→}$
+R′-X$\stackrel{一定条件}{→}$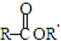 +NaX
+NaX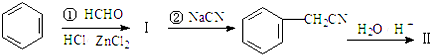 $\stackrel{NaOH}{→}$Ⅲ$\stackrel{一定条件}{→}$Ⅳ(C15H14O2)
$\stackrel{NaOH}{→}$Ⅲ$\stackrel{一定条件}{→}$Ⅳ(C15H14O2)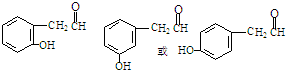 .
.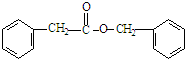 .
. .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com