
| A�� | ��������ѹ��ʱ�����淴Ӧ���ʾ����� | |
| B�� | 5 min��ƽ����Ӧ����v��X��=0.02 mol/��L•min�� | |
| C�� | ��ƽ������ϵ�м���l molM��s����ƽ�����淴Ӧ�����ƶ� | |
| D�� | �����������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬ |
���� 5min��ﵽƽ�⣬��ʱ����0.2mol Z����
X��g��+Y��g��?2Z��g��+M��s��
��ʼ 1 n 0
ת�� 0.1 0.1 0.2
ƽ�� 0.9 n-0.1 0.2
A����������ѹ��ʱ��ѹǿ����
B�����v=$\frac{��c}{��t}$���㣻
C���ı䴿���������ƽ�ⲻ�ƶ���
D��MΪ���壬�������������ڴﵽƽ��ǰΪ������
��� �⣺A����������ѹ��ʱ��ѹǿ�������淴Ӧ����ͬ�ȳ̶ȵ�����A����
B.5 min��ƽ����Ӧ����v��X��=$\frac{\frac{0.1mol}{2L}}{5min}$=0.01 mol/��L•min������B����
C����ƽ������ϵ�м���l molM��s����ƽ�ⲻ�ƶ�����C����
D��MΪ���壬�������������ڴﵽƽ��ǰΪ���������������������ٷ����仯ʱ��˵����Ӧ�ﵽƽ��״̬����D��ȷ��
��ѡD��
���� ���⿼�黯ѧƽ�⣬Ϊ��Ƶ���㣬�������ʼ��㡢ƽ���ƶ���ƽ���ж�Ϊ���Ĺؼ������ط�����Ӧ�������Ŀ��飬ע��MΪ���弰�����������䣬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͬ��ͬѹ�£���ͬ��������ʣ������ʵ���һ����� | |
| B�� | �����ʵ����ļ����һ����̼�����ķ�����ǰ�ߴ��ں��� | |
| C�� | 1Lһ����̼����һ����1L����������С | |
| D�� | ��ͬ�����µ�һ����̼�͵����������������ȣ�������Ҳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��Ӧ����v | B�� | ��ѧƽ�ⳣ��K | ||
| C�� | ������ʵĵ���ƽ�ⳣ��K | D�� | ˮ�����ӻ�����Kw |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ı���ϵ�¶ȣ���ϵ��ɫһ�������仯 | |
| B�� | ������ı�Ũ����һ������ʹ����ϵ��ɫ���������ƽ��һ������ | |
| C�� | ��������HI���壬��HI��ת���ʽ���С | |
| D�� | �¶Ȳ���ʱ������ϵ��ɫ��dz��������Ӧ���ʺ��淴Ӧ���ʶ�����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
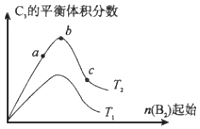
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ͻ��Ӳ��һ��ȸ���ֽ����ĵ� | B�� | �Ͻ��п��ܺ��зǽ���Ԫ�� | ||
| C�� | �Ͻ��п϶����н���Ԫ�� | D�� | �Ͻ���۵�һ��ȸ���ֽ����ĵ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
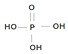 ��Ϊ��Ԫ��ǿ�ᣩ�������������Ϊ�����������֮����ȥ����ˮ���ӵIJ����ṹ��ʽΪ
��Ϊ��Ԫ��ǿ�ᣩ�������������Ϊ�����������֮����ȥ����ˮ���ӵIJ����ṹ��ʽΪ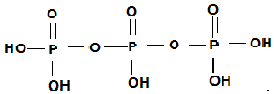 �������������dz��õ�ˮ���������仯ѧʽΪNa5P3O10��
�������������dz��õ�ˮ���������仯ѧʽΪNa5P3O10��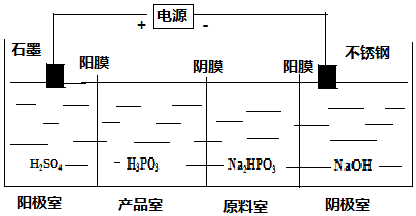
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��W ��X ��ɵĻ�����ķе��ܵ�����W��Y��ɵĻ�����ķе� | |
| B�� | ��������Ԫ�ص�ԭ�Ӱ뾶��СΪW��X��Y��Z | |
| C�� | Y����̬���⻯����ȶ��Ա�Z��ǿ | |
| D�� | W��Y��Z����Ԫ�ؿ��γ����ӻ����� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com