
| �������� | ���� | ���� | ���� | ���� |
| �е�/�� | ��88.6 | ��42.1 | ��0.5 | 36.1 |
| *ȼ����/kJ��mol��1 | 1 560.7 | 2 219.2 | 2 877.6 | 3 535.6 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���٢� | B���٢ڢ� | C���ܢݢ� | D���٢ܢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��Ũ������NaOH��Һ | B��KNO3����ˮ�� |
| C��NH4NO3����ˮ�� | D��CaO����ˮ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ�ʵ����
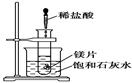
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�������ʵ������������������ֱ���ȫȼ�գ����߷ų������ࡡ |
| B����H+��aq��+OH-��aq��=H2O��l����H=-57.3kJ��mol-1��֪��������1 mol CH3COOH��ϡ��Һ�뺬1 mol NaOH��ϡ��Һ��ϣ��ų�������С��57.3 kJ�� |
C��300�桢30MPa�£���0.5molN2��g����1.5mol H2��g�������ܱ������г�ַ�Ӧ����NH3��g��������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��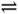 2NH3��g�� ��H=-38.6kJ��mol-1 2NH3��g�� ��H=-38.6kJ��mol-1 |
| D����C��ʯī��=C�����ʯ����H=" +1.90" kJ��mol-1��֪�����ʯ��ʯī�ȶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A�����ȵ�̿�������̼��Ӧ | B������ϡ����ķ�Ӧ |
| C��������������ķ�ĩ���Ȼ�茶����� | D��������Ʒ����ķ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������仯�����ʱ仯���ǻ�ѧ�仯 | B����ͬ��ʽ������ת��һ���ǻ�ѧ�仯 |
| C����ѧ��Ӧ�е������仯���������仯 | D�����ʷ�����ѧ�仯һ�����������仯 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

| A����Ӧ����е�������������������е������� |
| B������ӦΪ���ȷ�Ӧ |
| C���÷�Ӧ���淴Ӧ�����ȹ��� |
| D����ͼ�п��Կ�����HBr������һ������H2������ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com