
| A、H2O |
| B、NH4Cl |
| C、NaOH |
| D、Na2O2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、加浓氨水 |
| B、升高温度 |
| C、加NH4Cl溶液 |
| D、加NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 |
| B、50 |
| C、2.5×103 |
| D、104 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升温可以加快合成SO3的速率同时提高SO2的转化率 |
| B、寻找常温下的合适催化剂是未来研究的方向 |
| C、由于△H<0,△S<0,故该反应一定能自发进行 |
| D、当v(O2)生成?2v(SO3)消耗时,说明反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、方程式中化学计量数表示分子数 |
| B、△H2>0 |
| C、△H2=-△H1 |
| D、利用△H1,△H2可求出水的气化热 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠和水反应:2Na+2H2O═2Na++2OH-+H2↑ |
| B、FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
| C、铜和浓HNO3反应:3Cu+8H++2NO3-═3Cu2++2NO2↑+4H2O |
| D、NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-═BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
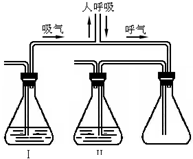 某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )
某化学兴趣小组为了证明人呼出的气体中含有CO2,设计了如图所示的实验装置.你认为锥形瓶Ⅰ、Ⅱ中应选用的一组试剂是( )| A. | B. | C. | D. | |
| 瓶Ⅰ | KOH | NaOH | 稀HCl | Na2SO4 |
| 瓶Ⅱ | NaOH | Ca(OH)2 | AgNO3 | BaCl2 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com