
| A.Cl2不但能与金属活动顺序表氢以前的金属反应,也能与金属活动顺序表氢以后的金属反应 |
| B.N2是大气中的主要成分之一,雷雨时,可直接转化为NO2 |
| C.硫是一种淡黄色的能溶于水的晶体,既有氧化性又有还原性 |
| D.硅是应用广泛的半导体材料,常温下只与氟气、氢氟酸反应 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.水泥具有水硬性 |
| B.水泥是一种纯净物 |
| C.水泥是水下工程必不可少的材料 |
| D.水泥、沙子和水的混合物叫混凝土 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
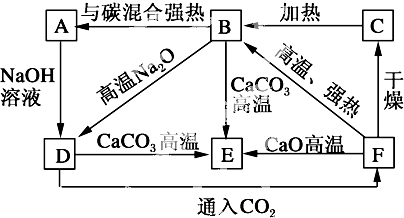
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.利用电解的方法可以从海水中获取淡水 |
| B.海水蒸发制海盐的过程只发生了化学变化 |
| C.从海水中可以得到NaCl,电解熔融NaCl可制备Cl2 |
| D.海水中含有钾元素,只需经过物理变化可以得到钾单质 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3+92.4KJ)在化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。
2NH3+92.4KJ)在化学工业和国防工业具有重要意义。工业合成氨生产示意图如图所示。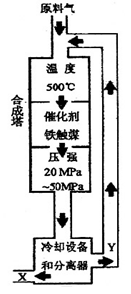
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
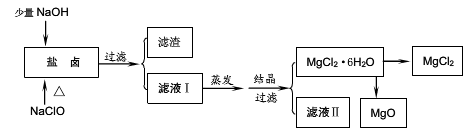
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
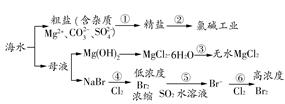
| A.过程①的提纯是物理过程,过程②通过氧化还原反应可产生2种单质 |
| B.在过程③中将MgCl2·6H2O灼烧即可制得无水MgCl2 |
| C.在过程④、⑥反应中每氧化0.2 mol Br-,需消耗2.24 L Cl2 |
| D.过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com