
硫酸亚铁(FeSO4·7H2O)是一种重要的食品和饲料添加剂。实验室通过如下实验由废铁屑制备FeSO4·7H2O晶体:
①将5% Na2CO3溶液加入到盛有一定量废铁屑的烧杯中,加热数分钟,用倾析法除去Na2CO3溶液,然后将废铁屑用水洗涤2 ~ 3遍;
②向洗涤过的废铁屑中加入过量的稀硫酸,控制温度在50 ~ 80℃之间至铁屑耗尽;
③趁热过滤,将滤液转入到密闭容器中,静置、冷却结晶;
④待结晶完毕后,滤出晶体,用少量冰水洗涤2 ~ 3次,再用滤纸将晶体吸干;
⑤将制得的FeSO4·7H2O晶体放在一个小广口瓶中,密闭保存。
请回答下列问题:
(1)实验步骤①的目的是 ,加热的作用是 。
(2)实验步骤②明显不合理,理由是 。
(3)实验步骤④中用少量冰水洗涤晶体,其目的是 ; 。
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
氢能源是一种重要的清洁能源。现有两种可产生H2的化合物甲和乙。将6.00 g甲加热至完全分解,只得到一种短周期元素的金属单质和6.72 LH2(已折算成标准状况)。甲与水反应也能产生H2,同时还产生一种白色沉淀物,该白色沉淀可溶于NaOH溶液。化合物乙在催化剂存在下可分解得到H2和另一种单质气体丙,丙在标准状态下的密度为1.25 g/L。请回答下列问题:
(1)甲的化学式是_________;乙的电子式是__________。
(2)甲与水反应的化学方程式是__________________________________-。
(3)气体丙与金属镁反应的产物是_______(用化学式表示)。
(4)乙在加热条件下与CuO反应可生成Cu和气体丙,写出该反应的化学方程式_________。
有人提出产物Cu中可能还含有Cu2O,请设计实验方案验证之_________________________。
(已知Cu2O+2H+==Cu+Cu2++H2O)
(5)甲与乙之间_______(填“可能”或“不可能)发生反应产生H2,判断理由是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:为使Fe3+、Fe2+、Zn2+较完全的形成氢氧化物沉淀,溶液的pH应分别为 3.7、9.6、4.4左右。某硫酸锌酸性溶液中含有少量Fe3+、Fe2+,为除去这些离子制得纯净的硫酸锌,应加入的试剂是( )
A.NaOH溶液 B.氨水
C.KMnO4、ZnCO3 D.H2O2、ZnO
查看答案和解析>>
科目:高中化学 来源: 题型:
在允许加热的条件下,只用一种试剂就可以鉴别硫酸铵、氯化钾、氯化镁、硫酸铝和硫酸铁溶液,这种试剂是 ( )
A NaOH B NH3·H2O C AgNO3 D BaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
铁氧体(Fe3O4)法是处理含铬废水的常用方法.其原理是:用FeSO4把废水中Cr2O72-离子还原为Cr3+离子,井通过调节废水的pH,使生成物组成符合类似于铁氧体(Fe3O4或FeO·Fe2O3)的复合氧化物(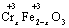 ·
· O)。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是( ) A.x=1,a=5 B.x=0.5 a=8 C.x=2,a=10 D.x=0.5,a=10
O)。处理含1 mol Cr2O72-的废水至少需要加入a mol FeSO4·7H2O,下列结论正确的是( ) A.x=1,a=5 B.x=0.5 a=8 C.x=2,a=10 D.x=0.5,a=10
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.蛋白质的水解可用于分离和提纯蛋白质
B.丙烯酸甲酯可通过缩聚反应生成高分子化合物
C.用乙醇和浓硫酸制备乙烯时,可用水浴加热控制反应的温度
 |
D.有机物 的核磁共振氢谱有两个峰,且峰面积之比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
已知分子式为C12H12的物质A的结构简式为 ,其苯环上的二溴代物
有9种同分异构体,由此推断A苯环上的四溴代物的同分异构体的数目有( )
A.9种 B.10种
C.11 种 D.12种
种 D.12种
查看答案和解析>>
科目:高中化学 来源: 题型:
海洋中资源丰富,以海水为原料可制得一系列产品,如下图所示:
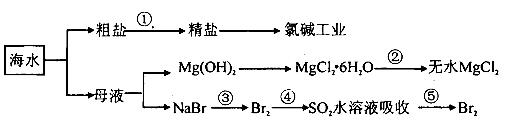
下列有关说法正确的是
A.第①步除去粗盐SO42-、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序为:
Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.将第②步结晶出的MgCl2 6H2O在空气中加热分解制备无水MgCl2
6H2O在空气中加热分解制备无水MgCl2
C.在第③④⑤步中溴元素均被氧化
D.电解饱和食盐水时,在阴极区生成NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于胶体的叙述不正确的是
A.胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9 ~ 10-7m之间
B.胶体是一种均一、稳定的混合物
C.用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同
D.Al(OH)3胶体能够吸附水中悬浮的固体颗粒沉降,达到净水目的
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com