
��ij�¶��£���������ʼ�����Ϊ1L���ܱ������а��±���ʾͶ�ϣ�������Ӧ��2SO2(g)+O2(g) 2SO3(g) ��H��0���ﵽƽ���������˵����ȷ����
2SO3(g) ��H��0���ﵽƽ���������˵����ȷ����
������� | �������� | ��ʼ���ʵ���/mol | ƽ��ʱSO3�����ʵ���/mol | ||
SO2 | O2 | SO3 | |||
�� | ���º��� | 2 | 1 | 0 | 1.2 |
�� | ���Ⱥ��� | 0 | 0 | 2 | a |
�� | ���º�ѹ | 2 | 1 | 0 | b |
A��ƽ��ʱSO3�����ʵ�����a��1.2��b��1.2
B����������ƽ�ⳣ����ͬ
C������ I��SO2��ת��������������SO3��ת����֮��С��1
D������ʼʱ���������г���1.0mol SO2 (g)��0.40mol O2(g)��1.40mol SO3 (g)�����ʱ����������

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ�˱��ظ�����һ����Ӧ�Բ������ۻ�ѧ�Ծ��������棩 ���ͣ�ʵ����
W�ṹ�к���������Ԫ������һ���������ϵ���Ҫ�ɷ�֮һ��W�ĺϳ�·������(���ֲ���Ͳ��ַ�Ӧ������ȥ)��
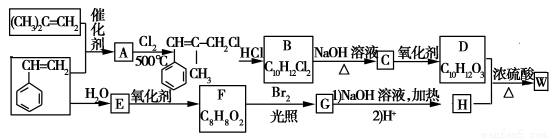
��֪����RCH===CH2��CH2===CHR��CH2===CH2��RCH===CHR��
��B�к˴Ź�������ͼ��ʾ��������6�ֲ�ͬ��������ԭ��
��D��H��ͬϵ��
��ش��������⣺
��1��G�����к��еĹ����������� ��
��2��A��B��Ӧ�������漰�ķ�Ӧ������ �� ��
��3��W�Ľṹ��ʽΪ ��
��4��B��C�Ļ�ѧ����ʽΪ ����D���ɸ߷��ӻ�����ķ���ʽΪ ��[
��5��ͬʱ��������������F��ͬ���칹���� ��(�����������칹)��
���ܷ���������Ӧ�����ܷ���ˮ�ⷴӦ��
���к˴Ź�������Ϊ5����Ϊ (д�ṹ��ʽ)��������֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ����5��ģ��һ���ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
2015������ר�����Ƴ�����һ��������ɳ��ij������������ӵ�أ��ֱ��Խ�������ʯīΪ�缫����AlCl4����A12C17�����л���������ɵ������Һ����ŵ繤��ԭ������ͼ��ʾ������˵������ȷ����

A���ŵ�ʱ����Ϊ������ʯīΪ����
B�����ʱ��������ӦΪ��Cn+AlCl4����e��=CnAlCl4
C���ŵ�ʱ�ĸ�����ӦΪ��Al��3e��+7AlCl4��=4A12C17��
D���ŵ�ʱ���л������������缫�����ƶ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꺣�ϼλ���ѧ�߶����������ƻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
ijȲ����������õ�2-�����飬��Ȳ����
A��2-��-1-��Ȳ B��2-��-3-��Ȳ C��3-��-1-��Ȳ D��3-��-2-��Ȳ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڿ�ǰ��ϰ��ѧ�Ծ��������棩 ���ͣ������
������һ�ּ��߷�չDZ���������Դ�����ѭ��������Ҫ���Ȼ�ѧ����ʽΪ��
��.SO2(g)+2H2O(l)+I2(g)��H2SO4 (l)+2HI(g) ��H��35.9 kJ/mol
��.2H2SO4(l)��2SO2(g)+O2(g)+2H2O(l) ��H��470kJ/mol
��.2HI(g)��H2(g)+I2(g) ��H��14.9kJ/mol
��1����Ӧ2H2(g)+ O2(g)��2H2O(l)�ġ�H�� mol��L��1��
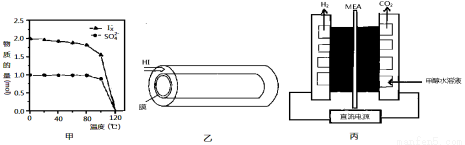
��2����Ӧ����Һ���з�����Ϊbensun��Ӧ����ˮ�м���1mol SO2��3mol I2���ڲ�ͬ�¶���ǡ����ȫ��Ӧ���ɵ�n(SO42��)��n(Ix��)�ı仯��ͼ�ס�
��Ix����x�� �����¶ȴﵽ120��ʱ���÷�Ӧ��������ԭ���� ��
��3����Ӧ������ͼ���н��У����еĸ߷���Ĥֻ��������ͨ�����߷���Ĥ��ʹ��Ӧ�̶� ___ (���������С�����䡱)���ڸ�װ����Ϊ�˽�һ�������ƽ��ʱHI�ķֽ��ʣ��������¶ȵ�Ӱ�죬�����Բ�ȡ�Ĵ�ʩΪ ��
��4��ͼ����һ���Ʊ�H2�ķ�����װ���е�MEAΪ��������ͨ���ĵ����Ĥ��
��д�������缫�ķ�Ӧʽ�� ��
�ڵ�����������������þ���Ͻ�(Mg17Al12)�����棬�Ͻ������õ�����һ�ֽ������⻯��(���������������Ϊ0.077)��һ�ֽ������ʣ��÷�Ӧ�Ļ�ѧ����ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڿ�ǰ��ϰ��ѧ�Ծ��������棩 ���ͣ�ѡ����
��N2��H2Ϊ��Ӧ�����A��ϡ����Ϊ�������Һ�����Ƴɹ̵�������ȼ�ϵ�ء�ԭ����ͼ��ʾ������˵������ȷ����

A��b�缫Ϊ����������������Ӧ
B��a�缫�����ķ�ӦΪN2+8H++6e-=2NH4+
C��A��Һ����������ΪNH4Cl
D������Ӧ����1molN2ʱ�������ĵ�H2Ϊ67.2L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڿ�ǰ��ϰ��ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵������ȷ����
A������ʽΪC2H4O2���л��ﲻһ��������
B���������еĻ�ѧ����������ʱ��һ��������ѧ�仯
C����������Al�ֱ�a��b����;����ȫת����;��a��;��b������H2
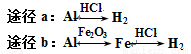
D��ֻ��һ��Ԫ�ص�����������һ��Ԫ�ص���������ɵ����ʲ�һ���Ǵ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���Ĵ��ɶ�ʯ����ѧ�߶�4���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
ҽ�����̷�(FeSO4•7H2O)������ȱ����ƶѪ����Чҩ��ij��ѧ��ȤС����̷����������µ�̽����
���Ʊ���Ʒ��
��С���ɷ���м(����������ͭ��������������)������ͼ��ʾװ���Ʊ� FeSO4 •7H2O���壬�������£�
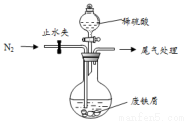
��1��Ԥ�������Ƚ�����м���뵽���� Na2CO3��Һ��ϴ�ӣ�Ŀ����__________ ��Ȼ����м��ˮϴ�� 2��3 �顣
��2����ϴ�Ӻ�ķ���м���뵽Բ����ƿ�У�������ͨ��N2
��3���ټ�������ϡ���ᣬ�����¶� 50�桫80��֮�䣬��ַ�Ӧ��Բ����ƿ��ʣ��Ĺ���Ϊ__________ ��ʵ���ҳ������軯����Һ���鷴Ӧ���ɵ�Fe2+��д���÷�Ӧ�����ӷ�Ӧ����ʽ��______________��
��4����ȡ��Ʒ�������裨3���з�Ӧ��Ļ�����м�����������ˮ�����ȹ��ˣ���ȴ�ᾧ���˳����壬��������ˮϴ�� 2��3 �Σ�������ֽ���������ɣ��ܱձ��档
���ⶨFeSO4 •7H2O ������
��1����ȡ������Ʒ 10.0g������������ϡ�����У���� 100mL ��Һ��ȷ��ȡ 25.00mL ��Һ������ƿ�У��� 0.1000mol/L KMnO4����Һ�ζ��ζ�3�Σ�ƽ������ 10.00mL��Һ������Ʒ�� FeSO4 •7H2O ����������Ϊ________ ��(��֪ Mr(FeSO4 •7H2O)=278)��
��2�����������ƫС����������ڶ���ʱ________(����ӡ������ӡ�)������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ʡ���������һ��ģ�����ۻ�ѧ�Ծ��������棩 ���ͣ������
�о�CO2�����öԴٽ���̼���Ĺ���������Ҫ���塣
��1����CO2�뽹̿��������CO��CO�����������ȡ�
��֪����Fe2O3(s) + 3C(ʯī) = 2Fe(s) + 3CO(g) ��H 1 = +489.0 kJ��mol��1
��C(ʯī) +CO2(g) = 2CO(g) ��H 2 = +172.5 kJ��mol��1
��CO��ԭFe2O3(s)���Ȼ�ѧ����ʽΪ ��
��2��������̼�ϳɼ״���̼���ŵ��·���CO2ת��Ϊ�״����Ȼ�ѧ����ʽΪ��
CO2(g) +3H2(g) CH3OH(g) +H2O(g) ��H
CH3OH(g) +H2O(g) ��H
�ٸ÷�Ӧ��ƽ�ⳣ������ʽΪK= ��
��ȡһ�����CO2��H2�Ļ�����壨���ʵ���֮��Ϊ1��3������������ܱ������У�����������Ӧ����Ӧ�����в�ü״������������(CH3OH)�뷴Ӧ�¶�T�Ĺ�ϵ��ͼ1��ʾ����÷�Ӧ�Ħ�H 0���>������<����������
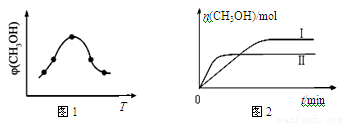
�������ֲ�ͬ�����·�����Ӧ�����CH3OH�����ʵ�����ʱ��仯��ͼ2��ʾ�����ߢ��Ӧ��ƽ�ⳣ����С��ϵΪK�� K��(�>������<������)���жϵ����� ��
��3����CO2Ϊԭ�ϻ����Ժϳɶ������ʡ�
�ٹ�ҵ������[CO(NH2)2]��CO2��NH3��һ�������ºϳɣ��䷴Ӧ����ʽΪ ����ʼ��̼��=3���з�Ӧ����ƽ��ʱCO2��ת����Ϊ60������NH3��ƽ��ת����Ϊ ��
�ڽ�����CO2ͨ�뱥�Ͱ�ˮ�пɵõ���NH4HCO3����֪������һˮ�ϰ�Kb=1.8��10��5��̼��һ�����볣��Kb=4.3��10��7����NH4HCO3��Һ�� ������ԡ��������ԡ��������ԡ�����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com