
| A. | 在元素周期表中,Y所在族的元素都是活泼金属元素 | |
| B. | 37Z原子核电子数为20 | |
| C. | X与Y能形成YX型化合物 | |
| D. | 在常温下,Z的单质与氢气一定能大量共存 |
分析 Z的单质通常为黄绿色气体,该气体为氯气,Z为Cl元素;X、Z同主族,则X为F元素;Z与Y能形成YZ型化合物,则Y的化合价为+1价,Y与Z同周期,则Y为Na元素,据此结合元素周期律知识进行判断.
解答 解:Z的单质通常为黄绿色气体,该气体为氯气,Z为Cl元素;X、Z同主族,则X为F元素;Z与Y能形成YZ型化合物,则Y的化合价为+1价,Y与Z同周期,则Y为Na元素,
A.Y为Na元素,处于ⅠA族元素,其中H元素为非金属元素,故A错误;
B.37Z原子为37Cl,其核电子数为17,故B错误;
C.X为F、Y为Na元素,二者能够形成离子化合物NaF,故C正确;
D.Z为Cl元素,其单质为氯气,氢气和氯气在常温下若光照会发生反应,故D错误;
故选C.
点评 本题考查了原子结构与元素周期律的关系,题目难度中等,“Z的单质通常为黄绿色气体”为突破口,明确原子结构与元素周期律的关系为解答关键,试题培养了学生的逻辑推理能力.


 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案科目:高中化学 来源: 题型:选择题
| A. | 氧化剂和还原剂的质量比1:2 | B. | SiO2是还原剂 | ||
| C. | 反应中有6g碳被氧化 | D. | 反应中生成28gCO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳:K+、Na+、SiO32-、Cl- | B. | 氨气:Ag+、Al3+、Na+、NO3- | ||
| C. | 氯化氢:Ca2+、Fe3+、NO3-、Cl- | D. | 氯气:Na+、Ba2+、I-、HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
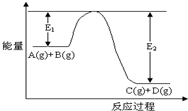 反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题
反应A(g)+B(g)?C(g)+D(g)过程中的能量变化如图所示,回答下列问题查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 改变条件,反应物的转化率增大,平衡常数也一定增大 | |
| B. | 常温下,V1L pH=12的NaOH溶液与V2L pH=2的HA溶液混合,若混合液显中性,则V1≤V2 | |
| C. | 在0.1mol•L-1 NaHCO3溶液中,加入少量NaOH固体,Na+和CO32-的离子浓度均增大 | |
| D. | 反应2NO2(g)?N2O4(g)△H<O,升高温度该反应平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
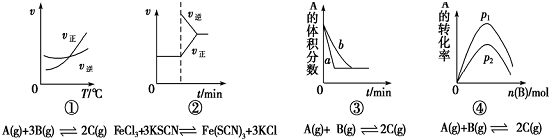
| A. | 图①是其他条件一定时反应速率随温度变化的图象,图象表明,较低温度下升温平衡逆向移动,较高温度下升温平衡正向移 | |
| B. | 图②是在平衡体系的溶液中加入少量KCl晶体后化学反应速率随时间的变化 | |
| C. | 图③可能是催化剂对化学平衡的影响,也可能是其它因素对化学平衡的影响 | |
| D. | 图④是一定条件下,向含有一定量A的容器中逐渐加入B时的图象,压强p1>p2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度/℃ | 400 | 500 | 830 | 1 000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com