
【题目】下列说法正确的是
A. SiO2是制造光导纤维的重要材料
B. SiO2溶于水生成硅酸
C. 晶体硅的化学性质不活泼,常温下不与任何物质发生反应
D. 硅酸钠是硅酸盐,俗称水玻璃,但不能溶于水
科目:高中化学 来源: 题型:
【题目】已知:![]() ,下列有机物能够合成
,下列有机物能够合成![]() 的组合是( )
的组合是( )
①1,3-丁二烯 ②2-甲基-l,3-丁二烯 ③1,3-戊二烯 ④2,3-二甲基-l,3-丁二烯
⑤2,3-二甲基-l,3-戊二烯 ⑥乙炔 ⑦丙炔 ⑧2-丁炔
A. ①、⑦及④、⑧ B. ⑤、⑥及③、⑧
C. ①、③及②、⑧ D. ②、⑧及④、⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据《科学快递》报道,研究人员拍摄到化学键形成过程中的过渡状态。化学键不存在于( )
A.原子与原子之间B.分子与分子之间
C.离子与离子之间D.离子与电子之间
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水三氯化铁呈棕红色、易潮解,在100 ℃左右时升华。设计如下实验,用来制取纯净、无水的FeCl3。

主要步骤:(1)加热浓盐酸和MnO2的混合物制取Cl2,请完成化学方程式:____________。
(2)________物质可净化Cl2,___________物质可干燥Cl2。
(3)净化干燥后的Cl2与Fe加热生成FeCl3
(4)过量的Cl2用NaOH溶液吸收,可制备________________。
【化学与生活】
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中进行反应:mX(g)+nY(g)![]() pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:

已知2 min内v(Q)=0.075 mol·L-1·min-1,v(Z)∶v(Y)=1∶2。
(1)试确定:起始时n(Y)=________,n(Q)=________。
(2)方程式中m=________,n=________,p=________,q=________。
(3)用Z表示2 min内的反应速率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】除去下列物质中的少量杂质(括号内的物质为杂质),所选用的试剂或方法不正确的是( )
A.CO2(SO2):饱和酸性KMnO4溶液
B.Cl2(HCl):饱和NaCl溶液
C.CO2(乙烯):通入溴的CCl4溶液
D.乙酸乙酯(乙酸):氢氧化钠溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是500 ℃时, 1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图。若在温度恒定,体积不变的容器中反应达到平衡,再充入NO2则,ΔH________(填“增大”、“减小”或“不变”,下同)。请写出NO2和CO反应的热化学方程式:__________。该反应能自发进行的主要原因为_____________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】B、D、C、A、E五种元素的原子序数顺序依次增大,其中只有E为金属元素,D、C元素在元素周期表中位置相邻,在一定条件下,B的单质可以分别和A、C、D的单质化合生成甲、乙、丙化合物,C的单质和D的单质化合可得丁,戊、己、庚均为化合物。已知乙、丙每个分子中均含有10个电子,下图为相互转化关系:
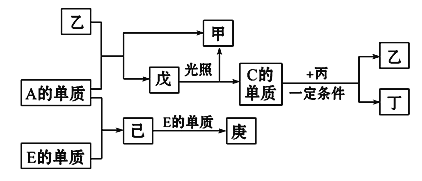
请回答下列问题:
(1)写出E的原子结构示意图_________________________。
(2)写出C、D氢化物的稳定性由强到弱的顺序____________。(用化学式表示)。
(3)A、B、D三种元素形成的化合物中,含有化学键的类型为___________。
(4)写出C与丙反应的化学反应方程式_________________________________。
(5)写出工业上从海水中制取A的离子反应方程式____________________________。
(6)工业上通过如下转化可制得含A元素的钾盐KAO3晶体:

①完成Ⅰ中反应的总化学方程式: ________
NaA+ H2O![]() NaAO3+
NaAO3+
②Ⅱ中反应过程能析出KClO3晶体而无其他晶体析出的原因是__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com