
��ҵ̼����(����ԼΪ98��)�к���Ca2+��Mg2+��Fe3+��Cl����SO42�������ʣ��ᴿ������·���£�
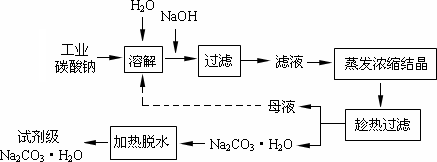
��̼���Ƶı�����Һ�ڲ�ͬ�¶�����������������ͼ��ʾ��
��25��ʱ�й����ʵ��ܶȻ�����(�����ܽ�ʱ��Һ������������Ũ�ȵij˻�)��

�ش��������⣺
(1)����NaOH��Һʱ���������ӷ���ʽΪ________��
25��ʱ������Mg2+��Fe3+����Һ�еμ�NaOH��Һ�������ֳ�����������Һ��pH��8ʱ��c(Mg2+)��c(Fe3+)��________��
(2)�����ȹ��ˡ�ʱ���¶�Ӧ������________��
(3)���˴ӡ���ɫ��ѧ���Ƕ����뽫��ĸҺ����������������ʾ����ѭ��ʹ�ã��������ʵ�ʹ�ҵ�������Ƿ����________����˵������________��
(4)��֪��Na2CO3��10H2O(s)��Na2CO3(s)��10H2O(g)����H����532.36 kJ��mol��1��Na2CO3��10H2O(s)��Na2CO3��H2O(s)��9H2O(g)����H����473.63 kJ��mol��1д��Na2CO3��H2O��ˮ��Ӧ���Ȼ�ѧ����ʽ________��
|
����(1)Fe3+��3OH����Fe(OH)3����MgCO3��2OH����Mg(OH)2����CO32��(2�֣���1��)��2.215��1021(2��) ����(2)����36��(2��) ����(3)�����У�(2��)������ĸҺ��ѭ��ʹ�ã�����Һc(Cl��)��c(SO42��)����������ò���Na2CO3�л�������(2��) ����(4)Na2CO3��H2O(s)��Na2CO3(s)��H2O(g)����H����58.73 kJ��mol��1(2��) |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
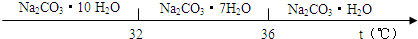
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�


| ���� | CaCO3 | MgCO3 | Ca��OH��2 | Mg��OH��2 | Fe ��OH��3 |
| Ksp | 4.96��10-9 | 6.82��10-6 | 4.68��10-6 | 5.61��10-12 | 2.64��10-39 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ʡ�彭��ѧ2009��2010ѧ��߶���ѧ����ĩ���Ի�ѧ���� ���ͣ�022
̼��������ֽ����������֯���Ƹ����ҵ����Ҫԭ�ϣ���ҵ̼����(����Լ98��)�к���Ca2+��Mg2+��Fe3+��Cl����SO![]() �����ʣ��ᴿ����·�����£���֪̼���Ƶ��ܽ��(S)���¶ȱ仯����������ͼ��ʾ��
�����ʣ��ᴿ����·�����£���֪̼���Ƶ��ܽ��(S)���¶ȱ仯����������ͼ��ʾ��

�ش��������⣺
(1)��������Ҫ�ɷ�Ϊ________��
(2)�����ȹ��ˡ���ԭ����________��
(3)����ĸҺ��ѭ��ʹ�ã����ܳ��ֵ����⼰��ԭ����________��
(
4)��֪��Na2CO3��10H2O(s)Na2CO3
��10H2O(s)д��Na2CO3��H2O��ˮ��Ӧ���Ȼ�ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ������ʡ��УЭ�������������һģ��ѧ�Ծ��������棩 ���ͣ�������
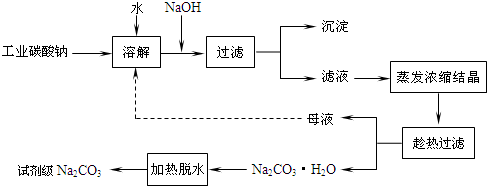
��ҵ̼���ƣ�����ԼΪ98�����к���Ca2+��Mg2+��Fe3+��Cl����SO42�������ʣ��ᴿ������·��ͼ��ʾ��

��̼���Ƶı�����Һ�ڲ�ͬ�¶���������������ͼ��ʾ��

���й����ʵ��ܶȻ�����
|
���� |
CaCO3 |
MgCO3 |
Ca��0H��2 |
Mg��OH��2 |
Fe��OH��3 |
|
Ksp |
4.96��10��9 |
6.82��10��6 |
4.68��10��6 |
5.61��10��12 |
2.64��10��39 |
�ش��������⣺
��1������NaOH��Һʱ����Ӧ�����ӷ���ʽΪ ������Mg2+��Fe3+����Һ�еμ�NaOH��Һ�������ֳ�����������Һ��pH=8ʱ��c��Mg2+����c��Fe3+��= ��
��2����ĸҺ���г��˺���Na+��CO32���⣬������ �����ӡ�
��3�����˴ӡ���ɫ��ѧ���Ƕ����뽫��ĸҺ�������������߽���ѭ��ʹ�á����������ʵ�ʹ�ҵ�������Ƿ���У� ������С������С�������˵�����ɣ� ��
��4����֪��Na2CO3��10H2O��s��=Na2CO3��s��+10H2O��g�� =+532.36 kJ��mol��1
=+532.36 kJ��mol��1
Na2CO3��10H2O��s��=Na2CO3��H2O��s��+9H2O��g��  =+473.63
kJ��mol��1
=+473.63
kJ��mol��1
д��Na2CO3��H2O��ˮ��Ӧ���Ȼ�ѧ����ʽ�� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com