
在温度T1和T2时,分别将0.50 mol CH4和1.2mol NO2充入1 L的密闭容器中发生反应:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g)△H=akJ/mol。测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g)△H=akJ/mol。测得有关数据如下表:
温度 | 时间/min 物质的量 | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列说法正确的是
A.T1>T2,且a>0
B.当温度为T2、反应进行到40 min时, x>0.15
C.温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新达到平衡时,n(N2)=0.70mol
D.温度为T1时,若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50 molH2O(g),反应开始时,ν(正)>ν(逆)
D
【解析】
试题分析:A.对于同一反应,当其它条件相同时,温度越高,反应速率越快,达到平衡所需要的时间就越短。因为在相同时间内反应在T2时物质的量变化的多,反应速率快,所以温度T1<T2,升高温度,达到平衡时CH4的物质的量多,说明升高温度,平衡逆向移动,逆反应方向是吸热反应,故该反应的正反应是放热反应,所以a<0,错误;B.反应温度在T1,反应时间是40min时就达到了平衡状态,由于温度T1<T2,所以当温度为T2、反应进行到40 min时,反应就处于平衡状态,外界条件不变,所以物质的平衡时的物质的量不变, x=0.15,错误;C.温度为T2时,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,假如平衡不发生移动,则重新达到平衡时,n(N2) =(0.50 mol —0.15mol)×2=0.70mol。而实际上,反应物物质的浓度呈比例增大,即增大了压强,由于该反应的正反应是气体体积增大的反应,增大压强,平衡向气体体积减小的逆反应方向移动,所以n(N2)<0.70mol,错误;D.温度为T1时,化学平衡常数K=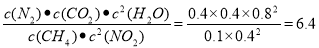 。若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50 molH2O(g),反应开始时,Qc=
。若起始时向容器中充入0.50 mol CH4(g)、0.50 molNO2(g)、1.0 mol N2(g)、2.0 molCO2(g)、0.50 molH2O(g),反应开始时,Qc=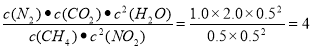 <6.4,说明反应未达到平衡,ν(正)>ν(逆),正确。
<6.4,说明反应未达到平衡,ν(正)>ν(逆),正确。
考点:考查温度对化学平衡的影响、反应热的判断、反应进行的方向的判断的知识。


科目:高中化学 来源:2014-2015黑龙江省绥化市三校高一上学期期末联考化学试卷(解析版) 题型:填空题
(10分)盐酸、硫酸和硝酸是中学阶段常见的“三大酸”。现就硫酸、硝酸与金属铜反应的情况,回答下列问题:
(1)工业上制备硫酸铜是利用废铜屑经灼烧后,在加热情况下跟稀硫酸反应,有关的化学方程式是 。不采用铜跟浓硫酸反应来制取硫酸铜的原因是
(2)在一定体积的10 mol·L-1的浓硫酸中加入过量铜片,加热使之反应,被还原的硫酸为0.9 mol。则浓硫酸的实际体积 (填“大于”、“等于”或“小于”)180 mL。
(3)若使剩余的铜片继续溶解,可在其中加入硝酸盐溶液(如KNO3溶液),则该反应的离子方程式为
(4)将8 g Fe2O3投入到150 mL某浓度的稀硫酸中,再投入7 g铁粉,充分反应后,收集到1.68 L H2(标准状况),同时,Fe和Fe2O3均无剩余,为了中和过量的硫酸,且使溶液中铁元素完全沉淀,共消耗4 mol·L-1的NaOH溶液150 mL。则原硫酸的物质的量浓度为
查看答案和解析>>
科目:高中化学 来源:2014-2015学年浙江省高三1月份阶段测试化学试卷(解析版) 题型:选择题
S2Cl2在合成橡胶、硬水软化等方面有着重要应用。将Cl2通入熔融的硫磺可制得S2Cl2,S2Cl2是黄红色油状发烟液体,遇水分解出无色有刺激性气味的气体,且溶液变浑浊。有关叙述正确的是
A.在周期表中,氯元素位于硫元素之后,所以Cl2的氧化性弱于硫单质
B.Cl2与硫磺的反应中,S2Cl2只是氧化产物
C.在常温常压下,硫磺是原子晶体,S2Cl2是分子晶体
D.S2Cl2与水反应时,既体现氧化性又体现还原性
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津南开区高三上学期第三次月考理综化学试卷(解析版) 题型:填空题
(18分)某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验I:制取NaClO2晶体
己知:NaClO2饱和溶液在温度低于38℃时析出品体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。利用下图所示装置进行实验。

(1)装置③的作用是 装置①的作用是
(2)装置②中制备ClO2的化学方程式为 ;产生ClO2的还原剂是装置④中制备NaClO2的化学方程式为
(3)从装置④反应后的溶液获得NaClO2晶体的操作步骤为:
①减压,55℃蒸发结晶:②趁热过滤;③ ;④低于60℃干燥,得到成品。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:①准确称取所得亚氯酸钠样品mg于小烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+4I-+4H+=2H2O+2I2+Cl-)。将所得混合液配成250mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,加几滴淀粉溶液,用c mol·L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得平均值为V mL(已知:I2+2S2O32-=2I-+S4O62-)。
(4)达到滴定终点时的现象为
(5)该样品中NaClO2的质量分数为 (用含m、c、V的代数式表示)。
(6)在滴定操作正确无误的情况下,此实验测得结果 (填“偏高”或“偏低”),原因用离子方程式表示为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年天津南开区高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
下列说法错误的是
A.K2FeO4能与水作用生成Fe(OH)3胶体和O2,可用于净化自来水并杀菌消毒
B.分散质粒子的直径:Fe(OH)3悬浊液>Fe(OH)3胶体>FeCl3溶液
C.若要除去CO2中含有的少量SO2气体,可通过盛有饱和NaHCO3溶液的洗气瓶
D.对“地沟油’’蒸馏可以获得汽油
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省攀枝花市高三上学期第二次统考理综化学试卷(解析版) 题型:选择题
下列反应中,反应后固体物质增重的是
A.氢气通过灼热的CuO粉末 B.将锌粒投入CuSO4溶液
C.CO2通过Na2O2粉末 D.将铜片投入FeCl3溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省达州市普高高三上学期第一次诊断理综化学试卷(解析版) 题型:选择题
下述实验能达到预期目的的是
编号 | 实验内容 | 实验目的 |
A | 准确称取氯化钾固体,放入到100mL的容量瓶中,加水溶解,振荡摇匀,定容 | 配制100mL一定浓度的氯化钾溶液 |
B | 下层液体从分液漏斗下端口放出,关闭活塞,换一个接收容器,上层液体继续从分液漏斗下端管口放出 | 取出分液漏斗中所需的上层液体 |
C | 向盛有沸水的烧杯中滴加FeCl3饱和溶液继续加热至溶液呈红褐色 | 制备Fe(OH)3胶体 |
D | 分别向2支试管中加入相同体积不同浓度的H2O2溶液,再向其中1支试管加入少量MnO2 | 研究催化剂对H2O2分解速率的影响 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市闸北区高三上学期期末化学试卷(解析版) 题型:选择题
可用下图所示装置制取、干燥、收集并吸收多余气体的是

A.浓氨水与氧化钙固体反应制氨气
B.稀硫酸与硫化亚铁固体反应制硫化氢
C.浓盐酸与次氯酸钙固体反应制氯气
D.饱和食盐水与电石反应制乙炔
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市普陀区高三一模化学试卷(解析版) 题型:选择题
甲烷与四氯化碳分子的空间构型相同,有关两者的比较中正确的是
A.甲烷与四氯化碳分子都是含有极性键的极性分子
B.甲烷与四氯化碳分子内的键角均为600
C.甲烷沸点低于四氯化碳,因为C—H键键长比C—Cl键短
D.甲烷分子比四氯化碳稳定,因为C—H键键能比C—Cl键大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com