
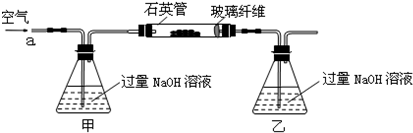
��15�֣��ס�����ͬѧΪ̽��SO2������Ա���ǿ�����ܷ�Ӧ���ɰ�ɫBaSO3����������ͼ��ʾװ�ý���ʵ�飨�г�װ�ú�A�м���װ�����ԣ��������Ѽ��飩
ʵ�����������
| ���� | ���� |
| �رյ��ɼУ��μ�һ����Ũ���ᣬ���� | A���а������ɣ�ͭƬ����������� B��������ð��������������ɫ���� C�в�����ɫ������Һ���Ϸ�����dz��ɫ������ʧ |
| ���ɼУ�ͨ��N2,ֹͣ���ȣ�һ��ʱ���ر� | ___________________ |
| ��B��C�зֱ�ȡ������ɫ��������ϡ���� | ��δ���ְ�ɫ�����ܽ� |
��1��A �з�Ӧ�Ļ�ѧ����ʽ��_________________��
��2��C�а�ɫ������__________________���ó��������ɱ���SO2����___________�ԡ�
��3��C��Һ���Ϸ�����dz��ɫ����Ļ�ѧ����ʽ��_____________________��
��4������B�в�����ϡ����ij���������ԭ����Ϊ�ǿ����гɷֹ�ͬ���ã�����Ϊ��ֻ�а������뷴Ӧ��
��Ϊ֤ʵ���ԵĹ۵㣬��ԭʵ������ϣ�����ԭ�в���֮ǰ����һ���������ò�����_____________;
����A��B������ϴ��ƿD��D��ʢ�ŵ��Լ���_____________��
�ڽ���ʵ�飬B������
| �� | ������ɫ���� |
| �� | ������ɫ���� |
�����ɫ���������־�������ϡ���ᡣ������ӷ���ʽ����ʵ��������ͬ��ԭ��_____��
��5���ϲ���4������ͬѧ�ķ����������顣B���������ɣ���C�в�����ɫ�������ɴ˵ó��Ľ�����_____________��
 ��������ϵ�д�
��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ���� | ʵ���¶�/�� | c��Na2S2O3��/mol?L-1 | c��H2SO4��/mol?L-1 |
| �� | 25 | 0.1 | 0.1 |
| �� | 25 | 0.1 | 0.2 |
| �� | 50 | 0.2 | 0.1 |
| �� | 50 | 0.1 | 0.1 |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
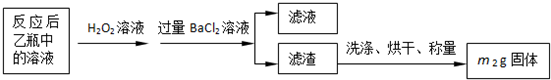
| 32m2 |
| 233m1 |
| 32m2 |
| 233m1 |
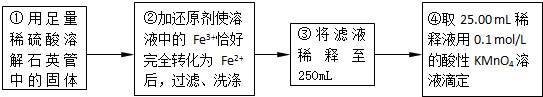
| ʵ����� | ��һ�� | �ڶ��� | ������ |
| ����KMnO4��Һ���/mL | 25.00 | 25.03 | 24.97 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 2Fe2O3+8SO2����
2Fe2O3+8SO2����  2Fe2O3+4SO2
2Fe2O3+4SO2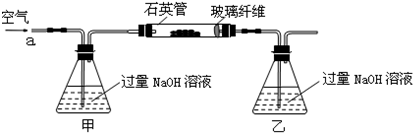
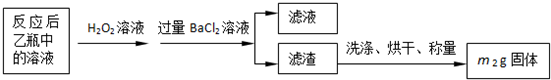
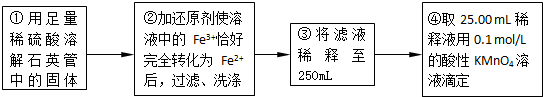
| ʵ����� | ��һ�� | �ڶ��� | ������ |
| ����KMnO4��Һ���/mL | 25.00 | 25.03 | 24.97 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ����������ģ ���ͣ��ʴ���
| ʵ���� | ʵ���¶�/�� | c��Na2S2O3��/mol?L-1 | c��H2SO4��/mol?L-1 |
| �� | 25 | 0.1 | 0.1 |
| �� | 25 | 0.1 | 0.2 |
| �� | 50 | 0.2 | 0.1 |
| �� | 50 | 0.1 | 0.1 |
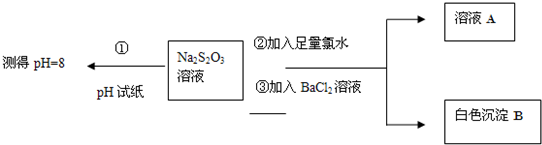
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�걱���ж������߿���ѧ��ģ�Ծ��������棩 ���ͣ������
| ʵ���� | ʵ���¶�/�� | c��Na2S2O3��/mol?L-1 | c��H2SO4��/mol?L-1 |
| �� | 25 | 0.1 | 0.1 |
| �� | 25 | 0.1 | 0.2 |
| �� | 50 | 0.2 | 0.1 |
| �� | 50 | 0.1 | 0.1 |
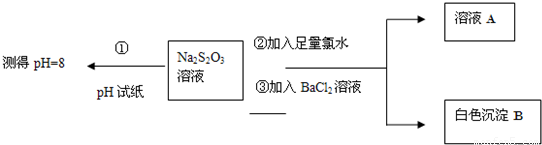
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com