
已知:NA表示阿伏加德罗常数,则下列说法不正确的是
A.31g白磷分子中所含p—p共价键数目为1.5NA
B.标准状况下,2.24LD2中所含中子的数目是0.2NA
C.常温常压下42g乙烯和丙烯的混合气体含氢原子数目为6 NA
D.常温下,向1L0.2mol/L的盐酸溶液通入氨气,当溶液PH=7时,溶液中NH4+的数目小于0.2NA
 习题精选系列答案
习题精选系列答案科目:高中化学 来源:2015-2016学年青海省高一下期末化学试卷(解析版) 题型:选择题
下列物质中,碱性最强的是( )
A. NaOH B. Mg(OH)2 C. Al(OH)3 D. KOH
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:实验题
高氯酸铵(NH4ClO4)常作火箭发射的推进剂。已知NH4ClO4在400℃时开始分解。某课题组设计实验探究NH4ClO4的分解产物(假设装置内药品均足量)。
(1)甲同学设计如图实验(部分夹持装置已省略):
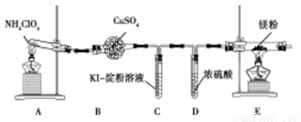
①若高氯酸铵分解有氯气生成,则可能观察到的现象是 ,写出产生该现象的离子方程式 。
②实验完毕后,取出E中硬质玻璃管中固体于试管中,滴加蒸馏水,产生的气体R能使红色湿润的石蕊试纸变蓝色。R的电子式为 。硬质玻璃管中固体与水反应放出R的化学方程式为 。
(2)乙同学认为,A中可能产生O2。为了验证他的猜想,选择上述部分装置和下列提供的装置进行实验:
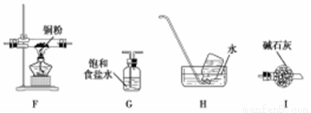
①按气流从左至右,装置的连接顺序为 。
②能说明有氧气的现象是 。
(3)通过查阅资料:NH4ClO4在℃时的分解产物为N2、Cl2、O2、H2O,写出高氯酸铵分解的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2017届湖南省长沙市高三上学期第二次周测化学试卷(解析版) 题型:选择题
日常生活离不开洗涤。下列使用的洗涤剂不正确的是
A.用纯碱溶液清洗餐具上的油污
B.用漂白液洗涤衣服上的字迹
C.用稀硫酸清洗水壶里的水垢
D.用汽油清洗皮肤上的油漆
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期第一次月考理综化学试卷(解析版) 题型:选择题
已知某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→ O2 ,则关于该反应体系说法错误的是
A.该反应的化学方程式为2H2CrO4+3H2O2=2Cr(OH)3+3O2↑+2H2O
B.该反应中的氧化剂是H2O2,还原产物是O2
C.氧化性:H2CrO4>O2
D.如反应转移了0.3mol电子,则产生的气体在标准状况下体积为3.36L
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:填空题
氮的氢化物——氨,是重要的化工原料,在工农业生产中有广泛的应用。而烟气中的NOx必须脱除(即脱硝)后才能排放。
(1)合成氨原料氢气的一个制备反应为:CO+H2O(g) CO2+H2
CO2+H2
①t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_________(填计算结果)。
②保持温度不变,向上述平衡体系中再加入0.1molCO,当反应重新建立平衡时,水蒸气的总转化率α(H2O)=______________________。
(2)NH3和O2在铂系催化剂作用下从145℃就开始反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g);
4NO(g)+6H2O(g);
△H=-905kJ·mol-1
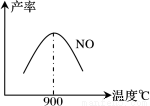
不同温度下NO产率如图所示。温度高于900℃时,
NO产率下降的原因____________。
(3)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(l);ΔH=-890.3kJ·mol-1
N2(g)+O2(g)=2NO(g); ΔH=+180kJ·mol-1
CH4可用于脱硝,其热化学方程式为______________________。
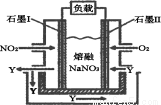
(4) 以NO2、O2、熔融NaNO3组成的燃料电池装置如下图所示,
在使用过程中石墨I电极反应生成一种氧化物Y,有关电极
反应可表示为_________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
同周期的X、Y、Z三种元素,已知最高价氧化物对应水化物的酸性由强到弱的顺序为HXO4>H2YO4>H3ZO4,则下列说法中,正确的是( )
A. 原子半径:X>Y>Z B. 非金属性:X>Y>Z
C. 气态氢化物的稳定性:ZH3>H2Y>HX D. 原子序数:Z>Y>X
查看答案和解析>>
科目:高中化学 来源:2015-2016学年吉林长春第十一中高一下期末考化学(解析版) 题型:选择题
可逆反应H2(g)+I2(g) 2HI(g)达到平衡状态时的标志是( )
2HI(g)达到平衡状态时的标志是( )
A.混合气体的体积恒定不变
B.混合气体的颜色不再改变
C.H2、I2、HI的浓度相等
D.I2在混合气体中的体积分数与H2在混合气体中的体积分数相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东省揭阳市高二期末统考理综化学试卷(解析版) 题型:实验题
Ⅰ.工业上制取硝酸的主要流程图如下图1:
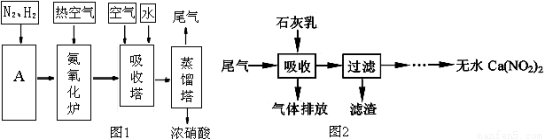
(1)工业合成氨的原料是N2和H2。装置A的名称是 ;其中N2可从空气中分离出来,方法是先将空气 ,然后 即可得到;H2可以水和天然气为原料在催化剂作用下高温制取,其化学方程式为 。
(2)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过反应CO(g)+H2O(g) CO2(g)+H2(g)来实现。已知1100 K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O)∶c(CO)不低于 。
CO2(g)+H2(g)来实现。已知1100 K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O)∶c(CO)不低于 。
Ⅱ.利用石灰乳来除去硝酸工业的尾气(含NO、NO2),既能净化尾气,又能获得应用广泛的Ca(NO2)2,其部分工艺流程如上图2。已知NO和NO2按1:1通入碱液中生成亚硝酸盐。
(1)上述工艺中采用气-液逆流接触吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是 ;滤渣可循环使用,滤渣的主要成分是 (填化学式)。
(2)该工艺需控制NO 和NO2 物质的量之比接近1:1。若n(NO):n(NO2)>1:1,则会导致 ;若n(NO):n(NO2)<1:1,则会导致 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com