
| A、NH3 |
| B、BCl3 |
| C、H2O |
| D、PCl3 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 5-3×1 |
| 2 |


科目:高中化学 来源: 题型:
| A、烧杯 酒精灯 试管 铁架台 漏斗 |
| B、滤纸 烧杯 试管夹 漏斗 玻璃棒 |
| C、漏斗 玻璃棒 烧杯 铁架台 滤纸 |
| D、滤纸 烧杯 试管夹 试管 铁架台 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、注射青霉素前要先做皮肤敏感试验 |
| B、运动员长期服用麻黄碱可提高成绩 |
| C、服用氢氧化钠溶液可中和过多的胃酸 |
| D、长期大量服用阿司匹林可预防感冒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、经常晒太阳 |
| B、适量饮用葡萄糖酸钙口服液 |
| C、经常饮用牛奶、豆奶 |
| D、经常饮用Ca2+含量高的硬水 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、8.0mol?L-1 |
| B、0.12mol?L-1 |
| C、0.8mol?L-1 |
| D、1.2mol?L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化性由强到弱顺序是:KMnO4>Cl2>Fe3+>I2 |
| B、还原性由强到弱顺序是:Mn2+>Cl->Fe2+>I- |
| C、I--与Fe3+能在溶液中发生氧化还原反应 |
| D、在溶液中可以发生2KCl+I2=Cl2+2KI反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅胶、浓硫酸、碱石灰、无水氯化钙都是实验室常用的干燥剂,它们都可以用来干燥NH3、Cl2、SO2、H2等气体 |
| B、将氯气和石灰乳混合可制漂白粉,其有效成分是氯化钙 |
| C、硅是一种良好的半导体材料,可用作做光电池和计算机芯片 |
| D、液氨可用作制冷剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温下,SiO2性质较稳定,不与所有的酸发生反应 |
| B、硅酸钠的水溶液俗称水玻璃,可作防火材料 |
| C、硅是一种亲氧元素,在地壳中的含量仅次于氧 |
| D、玻璃、陶瓷、水泥都属于硅酸盐产品 |
查看答案和解析>>
科目:高中化学 来源: 题型:
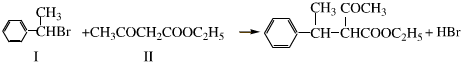
| H2 |
| 催化剂 |
| 浓硫酸 |
| △ |
| HBr |
 与一分子
与一分子 能发生类似①的反应,生成有机化合物Ⅴ,则Ⅴ的结构简式为
能发生类似①的反应,生成有机化合物Ⅴ,则Ⅴ的结构简式为查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com