
(15分)能源短缺是人类面临的重大问题。甲醇是一种可再生能源.具有广泛的开发和应用前景。因此甲醇被称为21世纪的新型燃料。
(1)已知在常温常压下:
①2CH3OH(I)十3O2(g)
2CO2(g)+4H2O(g) △H= _1275.6 kJ·mol—1
②H2O(I) === H2O(g) △H=+ 44.0 kJ.mol-1
写出表示甲醇燃烧热的热化学方程式 (2分).
(2)工业上一般采用下列两种反应合成甲醇:
反应A:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1
CH3OH(g)+H2O(g) △H1
反应B:CO(g)+2H2(g) CH3OH(g) △H2
CH3OH(g) △H2
取五份等体积CO2和H2的混合气体(物质的量之比均为1∶3),分别加入温度不同、容积相同的恒容密闭容器中,发生上述反应,反应相同时间后,测得甲醇的体积分数φ(CH3OH) 与反应温度T的关系曲线如下图所示,则上述CO2转化为甲醇的反应的△H1________0(填“>”、“<”或“=”)。(2分)

②对于反应A,若容器容积不变,下列措施可增加甲醇产率的是 (2分)。
A.升高温度 B.增加CO2的量
C.充入He,使体系总压强增大 D.按原比例再充入CO2和H2
③某温度下,将4mol CO和12mol H2,充人2L的密闭容器中,充分反应,达到平衡后,测得c(CO) =0.5 mol·L—1,,则该温度下该反应的平衡常数为 (2分)。
④.某种甲醇—空气燃料电池是采用铂作为电极,稀硫酸作电解质溶液。其工作时负极的电极反应式可表示为______________________ (2分)
(3)对燃煤烟气中的SO2、NO2设物质的量之比为1∶1,与一定量的氨气、空气反应,生成硫酸铵和硝酸铵的混合物作为副产品化肥。,则该反应的化学方程式为________ 。(3分)(4)在一定物质的量浓度的硝酸铵溶液中滴加适量的NaOH溶液,使溶液的pH=7,则
溶液中c(Na+)+c(H+)_____ c(NO3-)+c(OH-)(填写“>”“=”或“<”)(2分)
(1)CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) △H=-725.8 kJ·mol—1
(2)①< ②BD ③0.33 ④CH3OH-6e-+H2O=6H++CO2↑
(3)12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3。
(4)<
【解析】(1)燃烧热是在一定条件下1mol可燃物完全烧热生成稳定的氧化物是放出的能量。(①-②)/2的CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) △H=-725.8 kJ·mol—1。
(2)根据图像可知随着温度的升高,甲醇的含量逐渐增大,但当达到一定温度时反而降低,说明温度升高平衡向逆反应方向移动,过正反应是放热反应。反应A是体积减小的放热的可逆反应,高温不利于生成甲醇,充入He,使体系总压强增大但反应物的浓度并没有增大,所以平衡不移动,答案BD正确。
CO(g)+2H2(g) CH3OH(g)
CH3OH(g)
起始量(mol) 4 12 0
转化量(mol) 3 6 3
平衡量(mol) 1 6 3
所以平衡常数为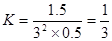 。
。
在反应中甲醇失去电子,所以负极的电极反应式CH3OH-6e-+H2O=6H++CO2↑
(3)根据所给反应物和生成物可写出反应式为12NH3+3O2+4SO2+4NO2+6H2O=4(NH4)2SO4+4NH4NO3。
(4)由电荷守恒知c(Na+)+c(H+)+c(NH4+)= c(NO3-)+c(OH-),所以c(Na+)+c(H+)< c(NO3-)+c(OH-)。


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 能源短缺是人类面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.
能源短缺是人类面临的重大问题.甲醇是一种可再生能源,具有广泛的开发和应用前景.| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com